تتم دراسة التسرطن باستخدام العديد من الاختبارات السمية المعيارية. يتم إجراء الجزء الأول من هذه الاختبارات في المختبر ، وإذا كانت إيجابية ، فإننا نواصل التجربة في الجسم الحي. يُطلق على هذا النهج التجريبي التدريجي اسم DECISION POINT APPROACH ، وهو سلسلة من التجارب التي تتوقف في نهاية كل تجربة لتحديد كيفية المضي قدمًا في التجربة. هناك خمس مراحل:
المرحلة أ: هيكل وخصائص المركب المسرطنة ؛
PHASEB: في هذه المرحلة من الاختبار قصير المدى في المختبر ، يتم استخدام خلايا الثدييات. الخلايا الكبدية الأكثر شيوعًا هي الخلايا الكبدية ، حيث يتم دراسة مدى إصلاح الضرر الذي تحدثه الخلايا الكبدية وفقًا لشدة الضرر الذي تسببه المادة. باختصار ، لا نحدد الضرر في حد ذاته ، بل نحدد مقدار نظام الإصلاح الذي تم تنشيطه بواسطة خلية الكبد.
الإجراء المنفذ هو تكوين 3 مزارع للخلايا الكبدية. في الثقافة الأولى ، تكون خلايا الكبد سليمة ، وفي الثانية يتم علاجها بمادة الاختبار ، وفي النهاية يتم علاجها في الثالثة بمادة ضابطة مسرطنة بالتأكيد.تحتوي هذه الثقافات الثلاث على قاعدة بيريميدين المشعة ، والتي هي tritiated thymidine ، والتي تعمل كعلامة.
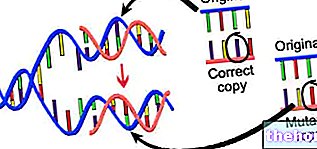
إذا تسبب المركب قيد الفحص في حدوث طفرة في الحمض النووي ، تستجيب الخلية لهذه المشكلة عن طريق تنشيط أنظمة الإصلاح. يتم قطع قطعة الحمض النووي التي خضعت للطفرة وبفضل عمل DNApolymerase ، يتم استبدال القطعة المفقودة بأخرى جديدة.للتصحيح ، يستخدم DNApolymerase القواعد الجديدة ، بما في ذلك thymidine tritiated. تم دمج قاعدة مشعة. يحدد تحليل النشاط الإشعاعي مستوى الطفرة في الخلايا المعالجة: كلما زاد النشاط الإشعاعي ، زادت طفرات الحمض النووي.
يتم أيضًا إجراء اختبارات في المرحلة B على البكتيريا ، لتتمكن من دراسة ما إذا كانت هناك أي طفرات عكسية. البكتيريا المستخدمة هي السالمونيلا الناقل بالفعل للطفرات. تتعلق الطفرة بتخليق الهيستيدين ، لذلك لا تستطيع السالمونيلا النمو بدون الهيستيدين. تؤخذ هذه المستعمرات البكتيرية جزئيًا لمعالجتها بمادة الاختبار ، وجزئيًا للتحكم السلبي وجزئيًا للتحكم الإيجابي ، ثم يتم اختبارها باستخدام مادة مسرطنة معروفة. إذا كانت مادة الاختبار هذه سامة جينية غير مباشرة ، فيجب إدخال الإنزيمات الأيضية في وسط المزرعة. في هذه المرحلة ، هناك 3 مزارع يتم زرع بذورها وتنميتها في أطباق بتري (لا يوجد هيستيدين في وسط الاستزراع). إذا لم يكن هناك أي طفرات بسبب المادة المسرطنة المراد اختبارها ، فمن الناحية النظرية يجب ألا يكون هناك أي طفرات على الأطباق . إذا كان هناك عمل مطفّر للمسرطن ، فربما يكون قد غيّر الطفرة الأولى وخلقت طفرة ثانية قادرة على إنماء البكتيريا على وسط مستنبت خالٍ من الهيستدين. في هذه الحالة ، الطفرة الثانية التي تعدل الطفرة الأولى و يأخذ اسم RETROMUTATION أخيرًا ، إذا حدث نمو كبير في piasta بتري ، فإن المادة المسرطنة تكون مباشرة.
دائمًا من خلال الاختبار في المختبر ، من الممكن تحديد سلامة الكروموسومات. يتم إجراء هذا الاختبار دائمًا على خلايا الثدييات ويستخدم لاختبار المواد السامة القادرة على إحداث طفرات في بعض الإنزيمات المسؤولة عن التخليق الحيوي للحمض النووي. المادة المراد اختبارها يخضع للتحليل في المختبر للتمكن من تحديد ما إذا كانت المادة قيد الفحص تؤثر على سلامة وعدد الكروموسومات الموجودة ، يتم استخدام اختبار النواة الدقيقة. النوى الدقيقة عبارة عن حويصلات تتشكل مع جزء من الكروماتين بالداخل. يمكن أن يكون الكروماتين المدمج في هذه النوى الدقيقة إما كروموسومات كاملة أو أجزاء من الكروموسومات. وتتكون النوى الصغيرة من الانقسام الخاطئ للخلية مما يؤدي إلى ظهور خلايا ابنة ذات مادة وراثية غير متساوية موزعة. ستكون نتيجة هذا الاختبار هي تحديد المواد التي تُعرف بالسموم الكاستوجينية والسموم المغزلية. تنتج المادة الكاستوجينية نوى صغيرة مع شظايا لا مركزية من الكروموسومات ، لذا فإن المادة تؤدي إلى حدوث كسر في الكروموسومات ، بدلاً من المادة السامة للمغزل التي تنتج من النوى الدقيقة الموجودة بداخلها توجد كروموسومات كاملة.
إذا تسببت المادة قيد الفحص في حدوث تسمم جيني في اختبار واحد أو أكثر ، يتم تعريف ذلك على أنه مشبوه للغاية ، لذلك ينتقل مباشرة إلى المرحلة (د) ، من ناحية أخرى ، إذا لم ينتج عن المادة التي تم اختبارها أي تأثير سام للجينات ، فإنها تنتقل إلى مرحلة الدراسة ج لأنه يمكن أن يكون المروج.
FASEC: في هذه المرحلة يمكن إجراء اختبارات في المختبر وفي الجسم الحي.
بالنسبة للاختبارات في المختبر ، يمكن إثبات إمكانية أن تكسر المادة المحفزة فجوة الوصلات بين الخلايا الطبيعية والخلايا السرطانية ، مع ما يترتب على ذلك من مرور المواد بين الخليتين.
اختبار في الجسم الحي هو تحريض أورام الجلد في الفئران. يتم وضع المادة المراد اختبارها مرتين أو ثلاث مرات في الأسبوع على جلد الفأرة. في غضون 2/3 أشهر ، إذا كانت هذه المادة محفزة ، فقد تكون هناك تكوينات الورم الحليمي. في الفئران ، تم أخذ معطيات رئيسية في الاعتبار: عدد الفئران المصابة بالأورام الحليمية وعدد الأورام الحليمية الموجودة في كل حيوان. إذا كانت المادة تعمل كمحفز وتطور ورمًا في الفأر المعالج ، فهذا يعني أنها بالفعل مادة لها تأثير محفز.
بمجرد الانتهاء من هذه الاختبارات ، ننتقل إلى الاختبارات المجراة على المدى الطويل.
FASED: في هذه المرحلة يتم اختبار جميع المركبات التي ثبت أنها مطفرة وجميع المركبات التي لا تثبت أنها مطفرة. الفحوصات التي يمكن إجراؤها مختلفة ، بعضها يتم إجراؤه على الكبد والرئة وأخيراً على الثدي.
يوضح اختبار الكبد ليس تكوين ورم حديث التكوين ، ولكن لتركيز الورم ، وبالتالي شيء يستعد ليصبح ورمًا. خلايا هذا التركيز هي بالفعل خلايا غير نمطية ، لذلك خضعت لطفرة وتستعد لتصبح خلايا ورمية. بعد فترة زمنية معينة ، وبفضل فحص تشريح الجثة ، يتم تحديد تكوين نقاط ما قبل الورم ، من خلال حساب عدد ومدى تكوينات ما قبل الورم.
يسمح اختبار الرئة بتحديد الورم الحميد ، وهو "شذوذ في خلايا أنسجة الرئة. وفي هذه الحالة أيضًا يتم فحص أنسجة رئة الجرذ بعد فترة طويلة إلى حد ما (أشهر) (يمكن التعرف على هذه الأورام بسهولة بسبب هي عقيدات بيضاء على الظهارة الرئوية).
يسمح اختبار الثدي بتحديد الأورام في الأنسجة الغدية. يتم دائمًا تقييم عدد الأورام الغدية المتكونة وعدد الحيوانات التي تظهر عليها الأورام الغدية.
إذا كانت هناك نتائج إيجابية من هذه الاختبارات ، فإن مادة الاختبار هي بالفعل مادة مسرطنة. في هذه المرحلة ، ننتقل إلى إجراء اختبارات باهظة الثمن مع أوقات تنفيذ طويلة جدًا.
PHASEE: في هذه المرحلة ، يخضع عدد متغير من الحيوانات ، من 20 إلى 50 ، لاختبارات طويلة المدى ، وهذه الاختبارات باهظة الثمن وتستغرق وقتًا طويلاً للحصول على نتائج معينة ؛ نتحدث عن حوالي 1/8 من حياة الحيوان ، ومن الممكن أن تموت بعض الحيوانات أثناء إجراء هذه الاختبارات ، لكن يتم دراستها دائمًا بتشريح الجثة والفحص النسيجي. الحيوانات المختارة هي دائمًا الجرذان والفئران ولا يعيش سوى 70-80٪ منها حتى نهاية الاختبارات طويلة المدى. يتم فطام الحيوانات المستخدمة فقط ، فكلما كانت أصغر سنًا ، كانت أكثر حساسية للعلاجات. خلال فترة الاختبار طويلة المدى ، يتم دعم الباحث دائمًا من قبل عالم إحصائي رياضي ، قادر على مراعاة جميع المعلومات التي تم جمعها وإعادة إنتاج البيانات المختلفة.
تبدأ الجرعات المختبرة على الحيوانات من الحد الأقصى للجرعة المسموح بها وجميع أجزائها الفرعية ، ويتم تقييم تفاعل الجرعة والاستجابة في الحيوان.
يجب أن تقترب الإدارة دائمًا من المسار الذي يمكن أن يتلامس من خلاله الرجل مع المادة قيد الفحص ، وبالتالي المسار الفموي أو الجلدي أو التنفسي ، بينما إذا تم اختبار التسرطن لدواء ما ، فمن المفيد أيضًا إجراء الحقن في الوريد.
مجموعات الحيوانات المختبرة هي 4 (50 حيوانًا لكل مجموعة):
- مجموعة NAIF التي لا يوجد لها علاج ؛
- مجموعة تعامل مع السيارة.
- مجموعة عولجت بمادة الاختبار ؛
- مجموعة تعامل مع مادة مسرطنة معروفة.
من المهم جدًا أن يكون عدد الحيوانات في كل مجموعة متساويًا قدر الإمكان ، وفي الواقع ، إذا كان هناك اختلاف كبير في عدد الحيوانات ، فقد يتضح أن الاختبار الإحصائي زائف.
التقييمات التي يتم إجراؤها هي:
- التكرار الكلي للأورام.
- تواتر بعض الأورام.
- تواتر الحيوانات المصابة بأكثر من نوع واحد من الأورام ؛
- عدد سرطانات الحيوانات.
في نهاية كل مراحل الدراسة هذه ، يتم تصنيف المادة في ترتيب تم وضعه من قبل IARC (الوكالة الدولية للبحث والتطوير حول السرطان) ووكالة حماية البيئة (EPA).
مقالات أخرى عن "دراسة وتقييم التسرطن"
- التسرطن
- السمية وعلم السموم
- علم السموم للدورة الإنجابية والتسبب بالمسخ