المكونات النشطة: تاكروليموس (تاكروليموس مونوهيدرات)
روتوبيك 0.03٪ مرهم
تتوفر ملحقات العبوات الأولية لأحجام العبوات:- روتوبيك 0.03٪ مرهم
- روتوبيك 0.1٪ مرهم
دواعي الإستعمال لماذا يستخدم روتويك؟ لما هذا؟
المادة الفعالة في Protopic ، tacrolimus monohydrate ، هي عامل مناعي.
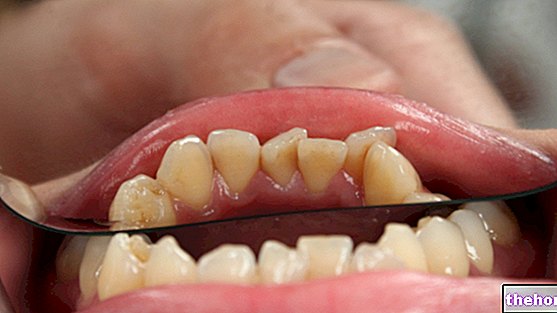
يوصف روتوبيك 0.03٪ مرهم لعلاج التهاب الجلد التأتبي المتوسط إلى الشديد (الإكزيما) عند البالغين الذين لا يستجيبون بشكل كافٍ أو الذين لا يتحملون العلاجات التقليدية مثل الكورتيكوستيرويدات الموضعية وفي الأطفال (سنتان وما فوق) الذين لم يستجيبوا. بشكل كافٍ للعلاجات التقليدية مثل الكورتيكوستيرويدات الموضعية.
إذا اختفى التهاب الجلد التأتبي المعتدل إلى الشديد أو اختفى تقريبًا بعد علاج التفاقم لمدة تصل إلى 6 أسابيع ، وإذا حدثت نوبات متكررة (4 أو أكثر في السنة) ، فيمكن الوقاية منها أو إطالة أمدها.لا تحدث مع استخدام روتوبيك. 0.03٪ مرهم مرتين في الأسبوع.
في التهاب الجلد التأتبي ، هناك رد فعل مفرط لجهاز المناعة في الجلد مما يسبب التهاب الجلد (الحكة ، الاحمرار ، الجفاف) ، يعدل بروتوبيك الاستجابة المناعية غير الطبيعية ويخفف التهاب الجلد والحكة.
موانع الاستعمال عند عدم استعمال روتويك
لا تستخدم بروتوبيك
- إذا كنت تعاني من حساسية (شديدة الحساسية) من عقار تاكروليماس أو أي من مكونات بروتوبيك أو المضادات الحيوية الماكروليد (مثل أزيثروميسين ، كلاريثروميسين ، إريثروميسين).
احتياطات للإستعمال ما الذي يجب أن تعرفه قبل تناول بروتوبيك
أخبر طبيبك
- إذا كان لديك فشل كبدي.
- إذا كان لديك أي أورام خبيثة في الجلد (الأورام) أو إذا كان لديك جهاز مناعي ضعيف (نقص المناعة) ، مهما كان السبب.
- إذا كنت تعاني من مرض جلدي خلقي مثل متلازمة Netherton ، السماك الرقائقي (تقشير واسع النطاق للجلد بسبب سماكة طبقة الجلد الخارجية) أو إذا كنت تعاني من احمرار الجلد المعمم (احمرار من التهاب وتقشر الجلد كله).
- إذا كنت تعاني من مرض الكسب غير المشروع الجلدي مقابل المضيف (رد فعل مناعي للجلد وهو أحد المضاعفات الشائعة في مرضى زراعة نخاع العظم).
- إذا كان لديك انتفاخ في العقد الليمفاوية في بداية العلاج ، إذا انتفخت الغدد الليمفاوية أثناء العلاج ب روتويك ، استشر طبيبك.
- إذا كان لديك آفات ملتهبة. لا تضع المرهم على الآفات المصابة.
- إذا لاحظت أي تغيير في مظهر بشرتك ، فيرجى إخبار طبيبك.
- إن سلامة استخدام روتويك على مدى فترة طويلة غير معروفة.عانى عدد قليل جدا من الأشخاص الذين استخدموا روتويك مرهم من أورام خبيثة (مثل الجلد أو الأورام اللمفاوية). ومع ذلك ، لم يظهر ارتباط مع العلاج بروتوبيك بمرهم .
- تجنب تعريض بشرتك لفترات طويلة لأشعة الشمس أو الضوء الصناعي مثل سرير التسمير. إذا كنت تقضي وقتًا في الهواء الطلق بعد وضع بروتوبيك ، فاستخدم واقيًا من الشمس وارتداء ملابس مريحة تحمي بشرتك من أشعة الشمس. كذلك ، استشر طبيبك للحصول على معلومات أخرى مناسبة طرق الحماية من أشعة الشمس: إذا تم وصف العلاج الشمسي لك ، أخبر طبيبك أنك تستخدم روتويك وأنه لا ينصح باستخدام روتويك والعلاج الشمسي في نفس الوقت.
- إذا وصف لك طبيبك بروتوبيك مرتين في الأسبوع لتجنب ظهور التهاب الجلد التأتبي من جديد ، فيجب إعادة تقييم حالتك من قبل طبيبك كل 12 شهرًا على الأقل حتى إذا كان المرض تحت السيطرة. في الأطفال ، يجب إيقاف علاج الصيانة بعد 12 شهرًا للتحقق مما إذا كانت هناك حاجة لاستمرار العلاج.
أطفال
- لم تتم الموافقة على استخدام مرهم روتويك للأطفال دون سن الثانية ، لذا لا ينبغي استخدامه في هذه الفئة العمرية ، يرجى استشارة طبيبك.
- لم يتم إثبات تأثير العلاج بالبروتويك على تطور الجهاز المناعي للأطفال ، وخاصة الشباب.
التفاعلات: الأدوية أو الأطعمة التي قد تغير من تأثير روتويك
أخبر طبيبك أو الصيدلي إذا كنت تتناول أو تناولت مؤخرًا أي أدوية أخرى ، بما في ذلك الأدوية التي تم الحصول عليها بدون وصفة طبية.
يمكنك استخدام الكريمات والمستحضرات المرطبة أثناء العلاج بـ روتويك ، ولكن يمكن وضعها فقط على نفس المنطقة المعالجة قبل ساعتين أو ساعتين بعد تطبيق روتويك.
لم يتم دراسة تأثير الاستخدام المتزامن لـ روتويك مع مستحضرات أخرى توضع على الجلد أو مع تناول الكورتيكوستيرويدات عن طريق الفم (مثل الكورتيزون) أو الأدوية التي تؤثر على جهاز المناعة.
بروتوبيك مع المشروبات الكحولية
أثناء استخدام روتويك ، قد يتسبب شرب المشروبات الكحولية في احمرار الوجه أو الجلد والإحساس بالحرارة
تحذيرات من المهم معرفة ما يلي:
الحمل والرضاعة
لا تستخدم روتويك إذا كنت حاملا أو مرضعة.
اسأل طبيبك أو الصيدلي للحصول على المشورة قبل تناول أي دواء
الجرعة وطريقة ووقت الإدارة كيفية استخدام Protopic: Posology
استخدم روتويك دائما كما أخبرك طبيبك. إذا كنت في شك ، استشر طبيبك أو الصيدلي.
- ضع طبقة رقيقة من روتويك على المناطق المصابة من الجلد.
- يمكن تطبيق روتويك على معظم سطح الجسم ، بما في ذلك الوجه والعنق والمناطق المعرضة لثني المرفقين والركبتين.
- تجنب استخدام المرهم في أنفك أو فمك أو عينيك. إذا تم وضع المرهم عن طريق الخطأ على هذه المناطق ، فستحتاج المنطقة إلى التنظيف تمامًا و / أو شطفها بالماء.
- لا تغطي المنطقة المصابة من الجلد بالضمادات أو الضمادات.
- اغسل يديك بعد وضع بروتوبيك ، إلا إذا كانت يديك أيضًا داخل المنطقة المراد علاجها.
- قبل تطبيق بروتوبيك بعد الاستحمام ، يجب التأكد من أن بشرتك جافة تمامًا.
استخدم في الأطفال (2 سنة وما فوق)
ضع مرهم روتوبيك 0.03٪ مرتين في اليوم لمدة ثلاثة أسابيع ، مرة في الصباح ومرة في المساء. بعد ذلك ، يجب استخدام المرهم مرة واحدة يوميًا على كل منطقة مصابة من الجلد حتى تلتئم الأكزيما.
الكبار (16 سنة وما فوق)
تتوفر قوتان من روتويك (روتوبيك 0.03٪ ومرهم روتوبيك 0.1٪) للمرضى البالغين (16 سنة فما فوق). سيقرر طبيبك الجرعة الأفضل لك.
بشكل عام ، يبدأ العلاج بـ روتوبيك 0.1٪ مرتين في اليوم ، مرة في الصباح ومرة في المساء ، حتى تختفي الأكزيما. بناءً على استجابة الأكزيما ، سيقرر الطبيب ما إذا كان سيتم تقليل تكرار الاستعمال أم إذا يمكن استخدام القوة الأقل (بروتوبيك 0.03٪).
عالج المناطق المصابة من الجلد حتى تلتئم الأكزيما ، بشكل عام ستلاحظ تحسنًا في غضون أسبوع واحد.استشر طبيبك حول أنواع العلاج الأخرى إذا لم تلاحظ أي تحسن ملحوظ بعد أسبوعين.
قد يصف لك طبيبك استخدام روتويك مرهم مرتين في الأسبوع بعد اختفاء أو اختفاء التهاب الجلد التأتبي تقريبًا (روتوبيك 0.03٪ للأطفال وبروتوبيك 0.1٪ للبالغين). ، الاثنين والخميس) على مناطق الجسم المصابة عادة بالتهاب الجلد التأتبي يجب أن تنقضي 2-3 أيام بين التطبيقات دون علاج روتوبيك.
إذا عادت الأعراض للظهور ، ارجع إلى استخدام روتويك مرتين في اليوم كما هو موضح أعلاه وحدد موعدًا مع طبيبك لفحص علاجك.
الجرعة الزائدة: ماذا تفعل إذا تناولت بروتوبيك أكثر من اللازم
إذا ابتلعت المرهم بالخطأ
إذا بلعت المرهم بالخطأ ، استشر طبيبك أو الصيدلي بأسرع ما يمكن ، ولا تحاول التسبب في التقيؤ.
إذا نسيت استخدام Protopic
إذا نسيت تطبيق المرهم في الوقت المحدد ، فقم بتطبيقه بمجرد أن تتذكر ، ثم استمر على النحو الموصوف.إذا كان لديك أي أسئلة أخرى حول استخدام روتويك ، اسأل طبيبك أو الصيدلي.
الآثار الجانبية ما هي الآثار الجانبية لبروتوبيك
مثل جميع الأدوية ، قد يتسبب بروتويك في حدوث آثار جانبية ، على الرغم من عدم حدوثها لدى الجميع.
شائعة جدًا (قد تظهر لدى أكثر من 1 من كل 10 أشخاص):
- إحساس بالحرقان والحكة
عادة ما تكون هذه الأعراض خفيفة إلى معتدلة وتختفي بشكل عام في غضون أسبوع واحد من بدء العلاج ب روتويك.
شائعة (قد تظهر لدى حتى 1 من كل 10 أشخاص):
- احمرار
- الشعور بالحرارة
- وجع
- زيادة حساسية الجلد (خاصة في الحرارة والبرودة)
- وخز في الجلد
- طفح جلدي عدوى جلدية محلية بغض النظر عن أسباب محددة ، بما في ذلك على سبيل المثال لا الحصر: بصيلات الشعر الملتهبة أو المصابة ، قروح البرد ، عدوى الهربس البسيط المعممة)
- يعد احمرار الوجه أو تهيج الجلد بعد تناول المشروبات الكحولية من التفاعلات الشائعة أيضًا
غير شائعة (قد تظهر لدى أقل من 1 من كل 100 شخص):
- حب الشباب
تم الإبلاغ عن إصابات في موقع التطبيق لدى الأطفال والبالغين بعد العلاج مرتين أسبوعياً. تم الإبلاغ عن القوباء ، وهي عدوى جلدية بكتيرية سطحية تسبب عادة بثور أو تقرحات على الجلد ، عند الأطفال.
تم الإبلاغ عن الوردية (احمرار الوجه) والتهاب الجلد الزائف الوردية ووذمة موقع التطبيق خلال مرحلة ما بعد التسويق.
منذ توفره في السوق ، أصيب عدد قليل جدًا من الأشخاص الذين استخدموا مرهم Protopic بأورام خبيثة (مثل الأورام اللمفاوية ، بما في ذلك الأورام اللمفاوية الجلدية أو سرطانات الجلد الأخرى). ومع ذلك ، لم يتم إثبات أو استبعاد وجود علاقة مع علاج روتويك المرهم بناءً على البيانات المتاحة حتى الآن.
التبليغ عن الأعراض الجانبية
إذا ظهرت لديك أي أعراض جانبية ، تحدث إلى طبيبك أو الصيدلي ، وهذا يشمل أي آثار جانبية محتملة غير مذكورة في هذه النشرة. يمكنك أيضًا الإبلاغ عن الآثار الجانبية مباشرةً عبر نظام الإبلاغ الوطني المدرج في الملحق الخامس. من خلال الإبلاغ عن الآثار الجانبية ، يمكنك المساعدة في توفير مزيد من المعلومات حول سلامة هذا الدواء.
انتهاء الصلاحية والاحتفاظ
يُحفظ بروتوبيك بعيدًا عن متناول الأطفال وبصرهم.
لا تستخدم روتويك بعد تاريخ انتهاء الصلاحية المدون على الأنبوب والكرتون بعد EXP ، يشير تاريخ انتهاء الصلاحية إلى اليوم الأخير من الشهر.
لا تخزن فوق 25 درجة مئوية.
لا ينبغي التخلص من الأدوية عن طريق مياه الصرف الصحي أو النفايات المنزلية ، اسأل الصيدلي عن كيفية التخلص من الأدوية التي لم تعد تستخدمها ، فهذا سيساعد في حماية البيئة.
ماذا يحتوي بروتوبيك
- العنصر النشط هو tacrolimus monohydrate. غرام واحد من روتوبيك 0.03٪ مرهم يحتوي على 0.3 ملغ من تاكروليموس (مثل تاكروليموس مونوهيدرات).
- المكونات الأخرى هي الفازلين الأبيض والبارافين السائل وكربونات البروبيلين وشمع العسل الأبيض والبارافين الصلب.
كيف يبدو روتوبيك وما هي محتويات العبوة
روتويك هو مرهم أبيض مائل للصفرة قليلاً. يتوفر في أنابيب تحتوي على 10 أو 30 أو 60 جرامًا من المرهم. قد لا يتم تسويق جميع أحجام العبوات. يتوفر روتويك بنوعين من القوة (روتوبيك 0.03٪ ومرهم روتوبيك 0.1٪).
نشرة حزمة المصدر: AIFA (وكالة الأدوية الإيطالية). تم نشر المحتوى في يناير 2016. المعلومات الموجودة قد لا تكون محدثة.
للوصول إلى أحدث إصدار ، يُنصح بالوصول إلى موقع AIFA (وكالة الأدوية الإيطالية). إخلاء المسؤولية والمعلومات المفيدة.
01.0 اسم المنتج الطبي
زيت بروتوبيك 0.03٪
02.0 التركيب النوعي والكمي
يحتوي 1 جم من مرهم روتوبيك 0.03٪ على 0.3 مجم من عقار تاكروليموس على هيئة تاكروليموس مونوهيدرات (0.03٪).
للحصول على قائمة كاملة من السواغات ، انظر القسم 6.1.
03.0 الشكل الصيدلاني
مرهم.
مرهم أبيض إلى أصفر قليلاً.
04.0 المعلومات السريرية
04.1 المؤشرات العلاجية
يشار إلى Protopic 0.03٪ مرهم في البالغين والمراهقين والأطفال من عمر سنتين.
علاج التفاقم
البالغون والمراهقون (الذين تبلغ أعمارهم 16 عامًا فأكثر)
علاج التهاب الجلد التأتبي المتوسط إلى الشديد عند البالغين الذين لا يستجيبون بشكل كافٍ أو الذين لا يتحملون العلاجات التقليدية مثل الكورتيكوستيرويدات الموضعية.
السكان من الأطفال (من سن 2 وما فوق)
علاج التهاب الجلد التأتبي المتوسط إلى الشديد عند الأطفال الذين فشلوا في الاستجابة للعلاجات التقليدية مثل الكورتيكوستيرويدات الموضعية.
علاج الصيانة
علاج التهاب الجلد التأتبي المعتدل إلى الشديد للوقاية من التفاقم ولإطالة الفترات الخالية من التفاقم في المرضى الذين يعانون من نوبات متكررة جدًا (4 مرات أو أكثر في السنة) والذين عانوا من استجابة أولية للعلاج لمدة أقصاها 6 أسابيع مع مرهم تاكروليموس مرتين يوميًا (اختفت الآفات أو اختفت تقريبًا أو ظهرت بشكل خفيف).
04.2 الجرعة وطريقة الإدارة
يجب أن يبدأ العلاج بالبروتوب من قبل أطباء ذوي خبرة في تشخيص وعلاج التهاب الجلد التأتبي.
يتوفر روتويك في مركبين ، روتوبيك 0.03٪ و روتوبيك 0.1٪ مرهم.
الجرعة
علاج التفاقم
يمكن استخدام روتويك لعلاج قصير الأمد ولعلاج متقطع طويل الأمد. لا يجب أن يكون العلاج طويل الأمد مستمرًا.
يجب أن يبدأ العلاج بالبروتويك عند أول ظهور للعلامات والأعراض. كل منطقة مصابة من الجلد يجب أن تعالج بـ روتويك حتى تختفي الآفات أو تكاد تختفي أو تظهر بشكل طفيف فقط. بعد ذلك ، يعتبر المرضى مؤهلين للعلاج المداومة (انظر أدناه). في أولى علامات الشفاء (تفاقم) أعراض المرض ، يجب استعادة العلاج.
استخدم في البالغين والمراهقين (الذين تتراوح أعمارهم بين 16 سنة وما فوق)
يجب أن يبدأ العلاج بـ روتويك 0.1٪ مرتين يومياً ويجب أن يستمر حتى زوال الآفة. إذا تكررت الأعراض ، يجب إعادة العلاج بـ روتوبيك 0.1٪ مرتين يومياً. إذا سمحت الظروف السريرية ، يجب بذل محاولة لتقليل تكرار التطبيقات أو استخدام القوة الأقل ، مرهم Protopic 0.03٪.
عادة ما يتم ملاحظة التحسن في غضون أسبوع واحد من بدء العلاج. إذا لم تظهر أي علامات تحسن بعد أسبوعين من العلاج ، فيجب التفكير في خيارات العلاج الأخرى.
السكان المسنين
لم يتم إجراء دراسات محددة على السكان المسنين. ومع ذلك ، فإن التجربة السريرية المتاحة لهذه المجموعة من المرضى لا تشير إلى الحاجة إلى تعديل الجرعة.
سكان الأطفال
يجب أن يستخدم الأطفال (2 سنة فأكثر) أقل تركيز: روتوبيك 0.03٪ مرهم.
يجب أن يبدأ العلاج مرتين يوميًا لمدة تصل إلى ثلاثة أسابيع.
بعد ذلك ، يجب تقليل تواتر التطبيقات إلى مرة واحدة يوميًا حتى تختفي الآفة (انظر القسم 4.4).
لا ينبغي استخدام مرهم Protopic في الأطفال الذين تقل أعمارهم عن سنتين حتى تتوفر المزيد من البيانات.
علاج الصيانة
المرضى الذين يستجيبون لمدة تصل إلى 6 أسابيع من العلاج بمرهم تاكروليموس مرتين يوميًا (اختفت الآفات أو اختفت تقريبًا أو كانت موجودة بشكل خفيف) مؤهلون للعلاج المداومة.
البالغون والمراهقون (الذين تبلغ أعمارهم 16 عامًا فأكثر)
يجب على المرضى البالغين استخدام مرهم روتوبيك 0.1٪.
يجب وضع مرهم بروتوبيك مرة واحدة في اليوم مرتين في الأسبوع (على سبيل المثال ، الاثنين والخميس) على المناطق المصابة عادة بالتهاب الجلد التأتبي لمنع حدوث نوبات.
بين التطبيقات يجب أن يكون هناك 2-3 أيام من التوقف عن العلاج روتويك.
بعد 12 شهرًا من العلاج ، يجب على الطبيب إعادة تقييم حالة المريض ليقرر ما إذا كان سيستمر في علاج الصيانة في حالة عدم وجود بيانات حول سلامة علاج الصيانة بعد 12 شهرًا.
إذا تكررت علامات التفاقم ، يجب استئناف العلاج مرتين يوميًا (انظر القسم السابق حول علاج التفاقم).
السكان المسنين
لم يتم إجراء دراسات محددة على كبار السن (انظر القسم السابق حول علاج التفاقم).
سكان الأطفال
يجب أن يستخدم الأطفال (2 سنة فأكثر) أقل تركيز: روتوبيك 0.03٪ مرهم.
يجب وضع مرهم بروتوبيك مرة واحدة يوميًا مرتين في الأسبوع (على سبيل المثال ، يومي الاثنين والخميس) على المناطق المصابة عادةً بالتهاب الجلد التأتبي لمنع تفاقم الالتهاب. بين التطبيقات يجب أن يكون هناك 2-3 أيام من التوقف عن العلاج روتويك.
يجب أن يشمل تقييم حالة الطفل بعد 12 شهرًا من العلاج وقف العلاج للتأكد من الحاجة إلى مواصلة هذا النظام وتقييم مسار المرض.
لا ينبغي استخدام مرهم Protopic في الأطفال الذين تقل أعمارهم عن سنتين حتى تتوفر المزيد من البيانات.
طريقة الإعطاء
يجب وضع طبقة رقيقة من مرهم روتويك على المناطق المصابة أو المصابة عادة من الجلد.
يمكن وضع مرهم بروتوبيك على جميع أجزاء الجسم ، بما في ذلك الوجه والعنق والمناطق المعرضة للثني ، باستثناء الأغشية المخاطية. لا ينبغي استخدام المرهم البروتوبيك مع ضمادات انسداد حيث لم يتم إجراء دراسات حول طريقة الإعطاء هذه (انظر القسم 4.4).
04.3 موانع الاستعمال
فرط الحساسية للمادة الفعالة أو الماكروليدات بشكل عام أو لأي من السواغات المدرجة في القسم 6.1.
04.4 تحذيرات خاصة واحتياطات مناسبة للاستخدام
أثناء استخدام مرهم Protopic يجب تقليل التعرض المفرط للجلد لأشعة الشمس ويجب تجنب استخدام الأشعة فوق البنفسجية المنبعثة من الاستلقاء تحت أشعة الشمس وعلاج UVB أو UVA مع psoralens (PUVA). (انظر القسم 5.3). يجب أن ينصح الطبيب المريض بالطريقة المناسبة للوقاية من الشمس ، مثل تقليل وقت التعرض للشمس ، واستخدام منتج مع واقي من الشمس ، وتغطية الجلد بالملابس المناسبة. لا ينبغي استخدام مرهم بروتوبيك على الآفات التي يُحتمل أن تكون خبيثة أو خبيثة.
يجب أن يراجع الطبيب التطور داخل المنطقة المعالجة لأي تغييرات بخلاف الأكزيما الحالية.
لا ينصح باستخدام مرهم تاكروليموس في المرضى الذين يعانون من عيوب حاجز الجلد مثل متلازمة Netherton أو السماك الرقائقي أو احمرار الجلد المعمم أو مرض الكسب غير المشروع مقابل المرض المضيف. قد تزيد حالات الجلد هذه من الامتصاص الجهازي للتاكروليموس. كما لا ينصح بإعطاء عقار تاكروليموس عن طريق الفم لعلاج هذه الحالات الجلدية. وقد وردت تقارير عن زيادة مستويات عقار تاكروليموس في الدم في ظل الظروف المذكورة أعلاه في بيئة ما بعد التسويق. ..
يجب توخي الحذر إذا تم تطبيق روتويك على المرضى الذين يعانون من تأثر شديد بالجلد لفترة طويلة من الزمن ، خاصة عند الأطفال (انظر القسم 4.2). يجب إعادة تقييم المرضى ، وخاصة مرضى الأطفال ، باستمرار أثناء العلاج ب روتويك لتقييم الاستجابة للعلاج وما إذا كان من الضروري مواصلة العلاج.
في مرضى الأطفال ، إعادة التقييم بعد 12 شهرًا يجب أن تشمل وقف العلاج بـ Protروتويك (انظر القسم 4.2).
إن احتمالية حدوث التثبيط المناعي الموضعي (مما يؤدي إلى التهابات الجلد أو السرطانات) غير معروف على المدى الطويل (أي على مدى عدة سنوات) (انظر القسم 5.1).
يحتوي بروتوبيك على المادة الفعالة تاكروليموس ، مثبط الكالسينيورين. في مرضى الزرع ، ارتبط التعرض الجهازي المطول لتثبيط المناعة بعد الإعطاء الجهازي لمثبطات الكالسينيورين بزيادة خطر الإصابة بالأورام اللمفاوية والأورام الخبيثة في الجلد. تم الإبلاغ عن حالات الأورام الخبيثة ، بما في ذلك الأورام الجلدية (مثل الأورام اللمفاوية للخلايا التائية الجلدية) وأنواع أخرى من الأورام اللمفاوية وسرطان الجلد في المرضى الذين يستخدمون مرهم تاكروليموس (انظر القسم 4.8). لا ينبغي أن يستخدم روتويك في المرضى الذين يعانون من نقص المناعة الخلقي أو المكتسب أو المرضى الذين يخضعون للعلاجات التي تسبب تثبيط المناعة.
لم يُظهر المرضى الذين عولجوا بالبروتوب المصاب بالتهاب الجلد التأتبي أي تراكيز جهازية كبيرة من عقار تاكروليموس.
كانت اعتلالات العقد اللمفية المبلغ عنها في التجارب السريرية غير شائعة (0.8٪). كانت معظم هذه الحالات مرتبطة بالعدوى (الجلد والجهاز التنفسي والأسنان) وتم حلها بـ "العلاج بالمضادات الحيوية المناسبة. مرضى الزرع الذين عولجوا بالعلاج المثبط للمناعة (مثل تاكروليموس المجموعي) لديهم خطر متزايد للإصابة بالأورام اللمفاوية ؛ لذلك ، المرضى الذين يتلقون روتوبيك الذين يتطورون يجب مراقبة تضخم العقد اللمفية للتأكد من أن اعتلال العقد اللمفية يجب أن يتم تقييمه ومراقبته. في حالة عدم وجود مسببات واضحة لاعتلال العقد اللمفية أو في وجود عدد كريات الدم البيضاء المعدية الحادة ، يجب التوقف عن تناول روتويك.
لم يتم إثبات تأثير العلاج بمرهم روتويك على التطور المناعي للأطفال دون سن الثانية (انظر القسم 4.1).
لم يتم تقييم مرهم بروتوبيك من حيث سلامته وفعاليته في علاج التهاب الجلد التأتبي المصاب. قبل بدء العلاج بمرهم روتويك ، يجب معالجة المناطق المصابة. المرضى الذين يعانون من التهاب الجلد التأتبي عرضة للإصابة بالتهابات الجلد السطحية. قد يترافق العلاج بـ روتويك مع زيادة خطر الإصابة بالتهاب الجريبات والالتهابات الفيروسية (التهاب الجلد بالهربس البسيط [إكزيما الحلأ] ، الهربس البسيط [قروح البرد] ، طفح كابوزي الحويري الشكل) (انظر القسم 4.8). في حالة وجود هذه الالتهابات ، يجب الموازنة بين المخاطر والفوائد المرتبطة باستخدام روتويك.
لا يمكن تطبيق المطريات على نفس المنطقة خلال ساعتين قبل أو بعد تطبيق مرهم روتوبيك.لم تتم دراسة الاستخدام المتزامن للمستحضرات الموضعية الأخرى. لا توجد خبرة في الاستخدام المتزامن للستيرويدات الجهازية أو العوامل المثبطة للمناعة.
يجب تجنب ملامسة العين والأغشية المخاطية. إذا تم تطبيقه عن طريق الخطأ على هذه المناطق ، يجب تنظيف المنطقة بعناية و / أو شطفها بالماء.
لم يتم دراسة استخدام روتويك المرهم في المرضى الذين يعانون من ضمادات انسداد ، ولا ينصح باستخدام الضمادات الإطباقية.
كما هو الحال مع جميع المنتجات الطبية الموضعية ، يجب على المرضى غسل أيديهم بعد التطبيق ما لم تكن اليدين أيضًا داخل المنطقة المراد علاجها.
يتم أيض عقار تاكروليموس على نطاق واسع في الكبد وعلى الرغم من انخفاض تركيزات الدم بعد العلاج الموضعي ، يجب استخدام المرهم بحذر في المرضى الذين يعانون من اختلال في وظائف الكبد (انظر القسم 5.2).
04.5 التفاعلات مع المنتجات الطبية الأخرى وأشكال التفاعل الأخرى
لم يتم إجراء دراسات تفاعل دوائي موضعي مع مرهم تاكروليموس.
لا يتأيض تاكروليموس في جلد الإنسان ؛ يشير هذا إلى عدم وجود تفاعلات محتملة عن طريق الجلد ، والتي يمكن أن تؤثر على عملية التمثيل الغذائي للتاكروليموس نفسه.
يتم استقلاب عقار تاكروليموس ، عند توفره بشكل نظامي ، عن طريق السيتوكروم الكبدي P450 3A4 (CYP3A4). التعرض الجهازي بعد التطبيق الموضعي لمرهم تاكروليموس منخفض (إريثروميسين ، إيتراكونازول ، كيتوكونازول وديلتيازيم) في المرضى الذين يعانون من مرض واسع الانتشار و / أو مرض احمرار الجلد يجب أن يتم بحذر.
سكان الأطفال
أجريت دراسة تفاعلية مع لقاح البروتين المتقارن ضد المجموعة الفرعية C من النيسرية السحائيةفي الأطفال الذين تتراوح أعمارهم بين 2 و 11 سنة. لم يكن هناك تأثير على الاستجابة الفورية للقاح ، أو على تكوين ذاكرة مناعية أو على المناعة الخلطية والخلطية (انظر القسم 5.1).
04.6 الحمل والرضاعة
خصوبة
لا توجد بيانات متاحة عن الخصوبة.
حمل
لا توجد بيانات كافية من استخدام مرهم تاكروليموس في النساء الحوامل ، وقد أظهرت الدراسات التي أجريت على الحيوانات سمية إنجابية بعد الإعطاء الجهازي (انظر القسم 5.3) ، والخطر المحتمل على البشر غير معروف.
لا ينبغي استخدام مرهم Protopic أثناء الحمل إلا في حالة الضرورة القصوى.
وقت الأكل
تشير البيانات البشرية إلى أنه بعد الإعطاء الجهازي ، يتم إفراز عقار تاكروليموس في حليب الثدي.على الرغم من أن البيانات السريرية أظهرت أن التعرض الجهازي بسبب تطبيق مرهم تاكروليموس ضئيل ، لا ينصح بالرضاعة الطبيعية.فترة العلاج بمرهم روتوبيك.
04.7 التأثيرات على القدرة على السياقة واستعمال الآلات
المرهم البروتوبيك ليس له تأثير أو تأثير ضئيل على القدرة على القيادة أو استخدام الآلات.
04.8 الآثار غير المرغوب فيها
خلال الدراسات السريرية ، عانى ما يقرب من 50 ٪ من المرضى من نوع من تهيج الجلد في منطقة التطبيق كرد فعل سلبي. الإحساس بالحرقان والحكة شائع جدًا ، وعادة ما يكون خفيفًا إلى متوسط الشدة ويميل إلى الشفاء في غضون أسبوع واحد من بدء العلاج. وهناك تفاعل شائع آخر لتهيج الجلد هو الحمامي. وقد لوحظ أيضًا بشكل شائع في منطقة التطبيق ، الإحساس بالحرارة ، الألم ، التنمل والطفح الجلدي. الشائع هو عدم تحمل الكحول (احمرار الوجه أو تهيج الجلد بعد تناول المشروبات الكحولية).
يمكن أن يزداد خطر الإصابة بالتهاب الجريبات وحب الشباب والالتهابات الفيروسية.
التفاعلات العكسية المشتبه في ارتباطها بالعلاج مذكورة أدناه ومقسمة حسب تصنيف الجهاز والنظام. يتم تعريف الترددات على أنها شائعة جدًا (1/10) ، شائعة (1/100 ،
* تم الإبلاغ عن ردود الفعل السلبية أثناء مراقبة ما بعد التسويق.
آخر التسويق
تم الإبلاغ عن حالات الأورام الخبيثة ، بما في ذلك الأشكال الجلدية (مثل الأورام اللمفاوية للخلايا التائية الجلدية) وأنواع أخرى من الأورام اللمفاوية وسرطان الجلد ، في المرضى الذين يستخدمون مرهم تاكروليموس (انظر القسم 4.4).
علاج الصيانة
في دراسة علاج الصيانة (العلاج مرتين أسبوعياً) عند البالغين والأطفال المصابين بالتهاب الجلد التأتبي المعتدل والشديد ، وجد أن الأحداث الضائرة التالية تحدث بشكل متكرر أكثر من المجموعة الضابطة: قوباء موقع التطبيق (7 ، 7٪ عند الأطفال) والتطبيق إصابات الموقع (6.4٪ في الأطفال و 6.3٪ في البالغين).
سكان الأطفال
تواتر ونوع وشدة ردود الفعل السلبية عند الأطفال مماثلة لتلك التي تم الإبلاغ عنها للبالغين.
الإبلاغ عن ردود الفعل السلبية المشتبه بها
يعد الإبلاغ عن التفاعلات العكسية المشتبه بها التي تحدث بعد ترخيص المنتج الطبي أمرًا مهمًا لأنه يسمح بالمراقبة المستمرة لتوازن الفوائد / المخاطر للمنتج الطبي. يُطلب من المتخصصين في الرعاية الصحية الإبلاغ عن أي ردود فعل سلبية مشتبه بها عبر نظام الإبلاغ الوطني. في "الملحق الخامس" .
04.9 جرعة زائدة
الجرعة الزائدة في التطبيق الموضعي غير محتمل.
في حالة الابتلاع ، قد تكون هناك حاجة لاتخاذ تدابير داعمة عامة ، بما في ذلك مراقبة العلامات الحيوية ومراقبة الحالة السريرية.بسبب طبيعة حامل المرهم ، لا يوصى بتحريض القيء وغسل المعدة.
05.0 الخصائص الصيدلانية
05.1 الخصائص الديناميكية الدوائية
المجموعة العلاجية الدوائية: أمراض جلدية أخرى. كود ATC: D11AH01.
آلية العمل والتأثيرات الدوائية
آلية عمل عقار تاكروليموس في التهاب الجلد التأتبي غير مفهومة تمامًا ، وبينما لوحظت آليات العمل التالية ، فإن أهميتها السريرية في التهاب الجلد التأتبي غير معروف.
من خلال ارتباطه بمناعة معينة من السيتوبلازم (FKBP12) ، يثبط عقار تاكروليموس مسارات الإشارات المعتمدة على الكالسيوم في الخلايا اللمفاوية التائية ، وبالتالي يمنع نسخ وتوليف IL-2 و IL-3 و IL-4 و IL-5 والسيتوكينات الأخرى مثل مثل GM-CSF و TNF-α و IFN-.
في المختبر، في خلايا لانجرهانز المعزولة من جلد الإنسان السليم ، يقلل عقار تاكروليموس من النشاط التحفيزي تجاه الخلايا التائية ، وقد ثبت أن عقار تاكروليموس يثبط إفراز الوسائط الالتهابية من الخلايا البدينة الجلدية ، والخلايا القاعدية ، والحمضات.
في الحيوانات ، قمع مرهم تاكروليموس التفاعلات الالتهابية في نماذج التهاب الجلد التجريبية والعفوية ، على غرار التهاب الجلد التأتبي البشري. لم يقلل مرهم تاكروليموس من سماكة الجلد ولا يسبب ضمور جلدي في الحيوانات.
في المرضى الذين يعانون من التهاب الجلد التأتبي ، يرتبط تحسن الآفات الجلدية أثناء العلاج بمرهم تاكروليموس مع انخفاض التعبير عن مستقبلات Fc على خلايا لانجرهانز وانخفاض نشاطها المفرط تجاه الخلايا التائية.لا يوجد تأثير لمرهم تاكروليموس على تخليق الكولاجين. في رجل.
الفعالية السريرية والسلامة
تم تقييم بروتوبيك من حيث الفعالية والأمان في أكثر من 18500 مريض عولجوا بمرهم تاكروليموس في الدراسات السريرية من المرحلة الأولى إلى الثالثة ، فيما يلي بيانات من ست دراسات سريرية رئيسية.
في دراسة عشوائية مزدوجة التعمية لمدة 6 أشهر ، تم تطبيق مرهم تاكروليموس 0.1٪ مرتين يوميًا للبالغين المصابين بالتهاب الجلد التأتبي المعتدل إلى الشديد ومقارنته بالعلاج الموضعي القائم على الكورتيكوستيرويد (0.1٪ هيدروكورتيزون الزبدات على الجذع والأطراف ، 1٪ خلات الهيدروكورتيزون على الوجه والرقبة). كانت نقطة النهاية الأولية هي درجة الاستجابة بعد ثلاثة أشهر ، والتي تم تحديدها على أنها النسبة المئوية للمرضى الذين تحسنوا بنسبة 60 ٪ على الأقل في mEASI (مؤشر معدل الشدة ومنطقة الأكزيما) في الشهر 3 من خط الأساس. كانت درجة الاستجابة في مجموعة tacrolimus 0.1٪ (71.6٪) أكبر بكثير مما كانت عليه في مجموعة الكورتيكوستيرويد الموضعية (50.8٪ ؛ p.
الجدول 1 الفعالية في 3 أشهر
§ العلاج بالكورتيكوستيرويد الموضعي = 0.1٪ هيدروكورتيزون الزبدات على الجذع والأطراف ، 1٪ أسيتات الهيدروكورتيزون على الوجه والرقبة
§ § قيم أعلى = تحسين أكبر
كانت نسبة حدوث وطبيعة معظم الأحداث الضائرة متشابهة في مجموعتي العلاج. حدث حرق الجلد ، والهربس البسيط ، وعدم تحمل الكحول (احمرار الوجه أو تهيج الجلد بعد شرب الكحول) ، والإحساس بالوخز ، وفرط الحساسية ، وحب الشباب والتهاب الجلد الفطري. مجموعة تاكروليموس. لم تكن هناك تغييرات ذات صلة سريريًا في القيم المختبرية أو العلامات الحيوية في أي من مجموعتي العلاج على مدار الدراسة.
في الدراسة الثانية ، تم علاج الأطفال الذين تتراوح أعمارهم بين 2-15 سنة المصابين بالتهاب الجلد التأتبي المتوسط إلى الشديد ، مرتين يوميًا لمدة ثلاثة أسابيع ، باستخدام مرهم تاكروليموس 0.03٪ ، مرهم تاكروليموس 0.1٪ ، أو مرهم أسيتات هيدروكورتيزون .1٪. كانت نقطة النهاية الأولية خلال الدراسة هي متوسط AUC (المنطقة الواقعة تحت المنحنى) كنسبة مئوية من درجة mEASI من خط الأساس. أظهرت نتائج هذه الدراسة العشوائية متعددة المراكز ، مزدوجة التعمية ، أن مرهم tacrolimus 0.03٪ و 0.1٪ ، أكثر فعالية بشكل ملحوظ (p.
الجدول 2 الفعالية في الأسبوع الثالث
§ قيم أقل = تحسن أكبر
كان معدل حدوث حرق الجلد الموضعي أعلى في مجموعة tacrolimus منه في مجموعة الهيدروكورتيزون. انخفضت الحكة بمرور الوقت في مجموعات tacrolimus ولكن ليس في مجموعة الهيدروكورتيزون. قيم المختبر أو العلامات الحيوية في كل مجموعة علاج على مدار الدراسة .
كان الهدف من الدراسة العشوائية الثالثة متعددة المراكز ، مزدوجة التعمية ، هو تقييم فعالية وسلامة مرهم تاكروليموس بنسبة 0.03٪ المطبق مرة أو مرتين يوميًا مقارنة بالتطبيق مرتين يوميًا لمرهم أسيتات الهيدروكورتيزون 1٪. التهاب الجلد التأتبي كانت مدة العلاج أكثر من ثلاثة أسابيع.
الجدول 3 الفعالية في الأسبوع الثالث
§ قيم أعلى = تحسن أكبر
تم تعريف نقطة النهاية الأولية على أنها النسبة المئوية للانخفاض في mEASI من خط الأساس إلى نهاية العلاج. لوحظ تحسن معتد به إحصائيًا مع مرهم tacrolimus 0.03٪ مرة أو مرتين يوميًا مقارنة بمرهم أسيتات الهيدروكورتيزون مرتين يوميًا (p
في الدراسة الرابعة ، المفتوحة ، ودراسة السلامة طويلة المدى ، تلقى ما يقرب من 800 مريض (بعمر أقل من عامين) مرهم تاكروليموس بنسبة 0.1 ٪ لمدة تصل إلى أربع سنوات ، إما بشكل متقطع أو مستمر ، مع تلقي 300 مريض العلاج لمدة ثلاث سنوات على الأقل و 79 مريضا تلقوا العلاج لمدة لا تقل عن 42 شهرًا. بناءً على التغيير من خط الأساس في درجة EASI ومنطقة الجسم المصابة ، أظهر المرضى ، بغض النظر عن العمر ، تحسنًا في التهاب الجلد التأتبي في جميع النقاط الزمنية اللاحقة. علاوة على ذلك ، لم يكن هناك دليل على فقدان الفعالية طوال مدة الدراسة السريرية.
تميل الوقوع الإجمالي للأحداث الضائرة إلى الانخفاض مع تقدم الدراسة لجميع المرضى بغض النظر عن العمر. كانت الأحداث الضائرة الثلاثة الأكثر شيوعًا التي تم الإبلاغ عنها هي الأعراض الشبيهة بالإنفلونزا (البرد ، والبرد ، والإنفلونزا ، والتهابات الجهاز التنفسي العلوي ، وما إلى ذلك) ، والحكة وحرق الجلد. في هذه الدراسة طويلة المدى ، لم يلاحظ أي أحداث سلبية لم يتم الإبلاغ عنها في الدراسات قصيرة المدى و / أو لوحظ في الدراسات السابقة.
تم تقييم فعالية وسلامة مرهم tacrolimus في علاج الصيانة من التهاب الجلد التأتبي الخفيف إلى الشديد في 524 مريضًا في تجربتين سريريتين من المرحلة الثالثة متعددة المراكز ذات تصميم مماثل في المرضى البالغين (16 عامًا) والمرضى البالغين ، على التوالي. -15 سنة).
في كلتا الدراستين ، خضع المرضى الذين يعانون من مرض مستمر لفترة تسمية مفتوحة (OLP) تم خلالها علاج الآفات المصابة بمرهم تاكروليموس مرتين لمدة تصل إلى 6 أسابيع.مرات في اليوم حتى وصل التحسن إلى درجة محددة مسبقًا (التقييم العالمي للباحث - IGA ≤ 2 ، أي الآفات اختفت ، أو اختفت تقريبًا أو كانت موجودة بشكل خفيف). بعد ذلك ، بدأ المرضى فترة من السيطرة على مرض التعمية المزدوجة (DCP) لمدة 12 شهرًا. 0.03٪ للأطفال) أو مركبة مرة واحدة في اليوم مرتين في الأسبوع ، يومي الاثنين والخميس.
عند حدوث اندلاع المرض ، عولج المرضى بعلامة مفتوحة بمرهم تاكروليموس مرتين يوميًا لمدة تصل إلى 6 أسابيع حتى عادت درجة IGA إلى ≤2.
كان الهدف الأساسي في كلتا الدراستين هو تقييم عدد حالات تفاقم المرض التي تتطلب "تدخلًا علاجيًا جوهريًا" خلال فترة DCP ، والتي تم تعريفها على أنها تفاقم مع IGA من 3-5 (أي درجة مرض معتدلة وحادة وشديدة جدًا). خلال اليوم الأول من التفاقم ، الذي يتطلب أكثر من 7 أيام من العلاج. أظهرت الدراستان فائدة كبيرة من العلاج مرتين أسبوعياً بمرهم تاكروليموس على نقاط النهاية الأولية والثانوية الرئيسية على مدى 12 شهرًا. التهاب الجلد التأتبي: في التحليل الفرعي للسكان للمرضى المصابين بالتهاب الجلد التأتبي المعتدل إلى الشديد ، ظلت هذه الفروق ذات دلالة إحصائية (الجدول 4) ، ولم يلاحظ في هذه الدراسات أي أحداث سلبية لم يتم الإبلاغ عنها سابقًا.
الجدول 4 الفعالية (فئة سكانية فرعية متوسطة إلى شديدة)
DE: تفاقم المرض
ص.
أجريت دراسة عشوائية مزدوجة التعمية لمدة 7 أشهر على مجموعات متوازية من مرضى الأطفال (2-11 سنة) المصابين بالتهاب الجلد التأتبي المتوسط إلى الشديد. في ذراع واحدة ، عولج المرضى بـ روتوبيك 0.03٪ مرهم (ن = 121) مرتين يومياً لمدة 3 أسابيع ثم مرة واحدة يومياً حتى اختفاء الآفات. في ذراع التحكم ، عولج المرضى بمرهم 1٪ هيدروكورتيزون أسيتات (HA) للرأس والرقبة و 0.1٪ مرهم هيدروكورتيزون الزبدات للجذع والأطراف (ن = 111) مرتين يوميًا لمدة أسبوعين ثم باستخدام HA مرتين يوميًا على جميع الأصناف. المناطق المتأثرة. خلال هذه الفترة ، تلقى جميع المرضى والأشخاص الضابطة (ن = 44) تحصينًا أوليًا ومُعززًا بلقاح مترافق بالبروتين ضد المجموعة الفرعية C من النيسرية السحائية.
كانت نقطة النهاية الأولية للدراسة هي معدل الاستجابة للتلقيح ، والذي تم تعريفه على أنه النسبة المئوية للمرضى الذين يعانون من عيار الجسم المضاد للجراثيم في الدم (SBA) ≥8 في زيارة الأسبوع الخامس. أظهر "تحليل معدل الاستجابة في الأسبوع الخامس" التكافؤ بين العلاج المجموعات (هيدروكورتيزون 98.3٪ ، مرهم تاكروليموس 95.4٪ ، 7-11 سنة: 100٪ في كلا الذراعين) النتائج في المجموعة الضابطة كانت متشابهة.
لم تتأثر الاستجابة الأولية للتطعيم.
05.2 خصائص حركية الدواء
أظهرت البيانات السريرية أن تركيزات عقار تاكروليموس في الدورة الدموية الجهازية بعد الإعطاء الموضعي تكون ضئيلة ، وعندما تكون قابلة للقياس ، تكون عابرة.
استيعاب
تشير البيانات الواردة من متطوعين أصحاء إلى أن هناك تعرضًا منهجيًا ضئيلًا أو معدومًا للتاكروليموس بعد التطبيق الموضعي الفردي أو المتكرر لمرهم تاكروليموس.
عولج معظم المرضى (البالغين والأطفال) من التهاب الجلد التأتبي بتطبيق واحد أو أكثر من مرهم تاكروليموس (0.03 - 0.1٪) والرضع من عمر 5 أشهر الذين عولجوا بمرهم تاكروليموس (0 ، 03٪) عالجوا تركيزات الدم في منطقة سطح الجسم ، إن التعرض الجهازي للتاكروليموس من بروتوبيك (أي AUC) أقل بحوالي 30 مرة من التعرض للجرعة المثبطة للمناعة الفموية في الكبد أو مرضى زرع الكلى.أقل تركيز دم من عقار تاكروليموس يمكن ملاحظة التأثير الجهازي به غير معروف.
لم يكن هناك دليل على التراكم الجهازي لـ tacrolimus في المرضى (البالغين والأطفال) الذين عولجوا لفترات طويلة (تصل إلى عام واحد) باستخدام مرهم tacrolimus.
توزيع
نظرًا لانخفاض التعرض الجهازي لمرهم tacrolimus ، فإن الارتباط العالي لـ tacrolimus (> 98.8 ٪) ببروتينات البلازما لا يعتبر ذا صلة سريريًا.
بعد التطبيقات الموضعية لمرهم التاكروليموس ، يتم إطلاق عقار تاكروليموس بشكل انتقائي على الجلد مع الحد الأدنى من الانتشار في الدورة الدموية الجهازية.
الأيض
لم يتم الكشف عن أي استقلاب للـ tacrolimus بواسطة جلد الإنسان. يتم استقلاب tacrolimus المتوفر جهازيًا في الغالب في الكبد بواسطة CYP3A4.
إزالة
في الإعطاء عن طريق الوريد ، وجد أن عقار تاكروليموس هو دواء بطيء معدل الإطراح.
متوسط تخليص الجسم حوالي 2.25 لتر / ساعة. قد يتم تقليل التخلص الكبدي من عقار تاكروليموس المتوفر جهازيًا في الأشخاص الذين يعانون من اختلال كبدي حاد ، أو في الأشخاص الذين يتم علاجهم بشكل متزامن مع الأدوية التي تعتبر مثبطات قوية لـ CYP3A4.
بعد التطبيقات الموضعية المتكررة للمرهم ، قُدر متوسط عمر النصف للتاكروليموس بـ 75 ساعة عند البالغين و 65 ساعة عند الأطفال.
سكان الأطفال
تشبه الحرائك الدوائية لـ tacrolimus بعد التطبيق الموضعي تلك التي تم الإبلاغ عنها عند البالغين ، مع الحد الأدنى من التعرض الجهازي وعدم وجود دليل على التراكم (انظر أعلاه).
05.3 بيانات السلامة قبل السريرية
السمية بعد العلاجات المتكررة والتحمل الموضعي
وجد أن التطبيق الموضعي المتكرر لمرهم تاكروليموس أو مركبته على الجرذان والأرانب والخنازير الصغيرة مرتبط بتغيرات جلدية خفيفة مثل الحمامي والوذمة والحطاطات.
في الجرذان ، أدى العلاج الموضعي طويل الأمد بالتاكروليموس إلى حالة من السمية الجهازية ، والتي تضمنت تغيرات في الكلى والبنكرياس والعينين والجهاز العصبي. ترجع التغييرات إلى التعرض العالي للقوارض الناتج عن الامتصاص العالي للتاكروليموس عبر الجلد. كان الاختلاف المنهجي الوحيد الذي لوحظ في الخنازير القزمية لتركيزات عالية من المرهم (3 ٪) هو زيادة الوزن الأقل قليلاً في الإناث.
تبين أن الأرانب حساسة بشكل خاص لإعطاء عقار تاكروليموس في الوريد ، حيث أظهروا تأثيرات سامة للقلب قابلة للعكس.
الطفرات
الإختبارات في المختبر و في الجسم الحي لم يشر إلى السمية الجينية المحتملة من tacrolimus.
السرطنة
لم تكشف دراسات السرطنة الجهازية في الفئران (18 شهرًا) والجرذان (24 شهرًا) عن وجود إمكانات مسرطنة لـ tacrolimus.
في دراسة السرطنة الجلدية التي استمرت 24 شهرًا والتي أجريت على الفئران مع تطبيق 0.1٪ مرهم ، لم تحدث أورام جلدية ، وفي نفس الدراسة لوحظ حدوث زيادة في الإصابة بسرطان الغدد الليمفاوية ، مرتبطة بالتعرض الجهازي العالي.
كجزء من دراسة السرطنة الضوئية ، عولجت الفئران البيضاء الخالية من الشعر بشكل مزمن باستخدام مرهم تاكروليموس والأشعة فوق البنفسجية. "زيادة في عدد الأورام. ليس من الواضح ما إذا كان تأثير عقار تاكروليموس ناتجًا عن تثبيط جهاز المناعة أو تأثير محلي. لا يمكن استبعاد الخطر على البشر تمامًا لأن احتمالية التثبيط المناعي المحلي في الاستخدام طويل الأمد لمرهم تاكروليموس غير معروف.
سمية الإنجابية
لوحظت سمية جنينية / جنينية في الجرذان والأرانب ، ولكن فقط عند الجرعات التي تسببت في سمية كبيرة للأم. تم الكشف عن انخفاض وظيفة الحيوانات المنوية في ذكور الجرذان عند تناول جرعات عالية من عقار تاكروليموس تحت الجلد.
06.0 المعلومات الصيدلانية
06.1 السواغات
الفازلين الأبيض البارافين السائل؛ كربونات البروبيلين؛ شمع العسل الأبيض ؛ بارافين صلب.
06.2 عدم التوافق
غير ذات صلة.
06.3 فترة الصلاحية
3 سنوات.
06.4 احتياطات خاصة للتخزين
لا تخزن فوق 25 درجة مئوية.
06.5 طبيعة العبوة الفورية ومحتويات العبوة
أنبوب مصفح ببطانة داخلية من البولي إيثيلين منخفض الكثافة ، مغلق بغطاء لولبي أبيض من البولي بروبيلين.
عبوات 10 جم و 30 جم و 60 جم. قد لا يتم تسويق جميع أحجام العبوات.
06.6 تعليمات الاستخدام والتداول
لا توجد تعليمات خاصة.
يجب التخلص من الأدوية غير المستخدمة والنفايات الناتجة عن هذا الدواء وفقًا للوائح المحلية.
07.0 حامل ترخيص التسويق
Astellas Pharma Europe B.V. - Sylviusweg 62، 2333 BE Leiden - هولندا
08.0 رقم ترخيص التسويق
EU / 1/02/201/001 Protopic 0.03٪ - AIC: 035575012
EU / 1/02/201/002 Protopic 0.03٪ - AIC: 035575024
EU / 1/02/201/005 Protopic 0.03٪ - AIC: 035575051
09.0 تاريخ أول تفويض أو تجديد التفويض
تاريخ أول تفويض: 28/02/2002
تاريخ التجديد: 11/20/2006