مقدمة
الصفائح الدموية أو الصفيحات هي أصغر العناصر الموجودة في الدم ، ولها شكل قرصي وقطرها بين 2 و 3 ميكرومتر. على عكس خلايا الدم البيضاء (أو الكريات البيض) وخلايا الدم الحمراء (أو كريات الدم الحمراء) ، فإن الصفائح الدموية ليست خلايا فعلية ، ولكنها أجزاء من السيتوبلازم من خلايا النواء الضخمة الموجودة في النخاع الأحمر. هذه ، بدورها ، مشتقة من السلائف التي تسمى الخلايا الأروماتية الضخمة وتظهر كخلايا كبيرة متعددة النوى (قطرها من 20 إلى 15 نانومتر) ، والتي بعد مراحل مختلفة من النضج تخضع لظواهر التفتت السيتوبلازمي ، والتي تنشأ من 2000 إلى 4000 صفيحة دموية. وبالتالي ، فإن الصفيحات خالية من النواة (مثل خلايا الدم الحمراء) ومن الهياكل مثل الشبكة الإندوبلازمية وجهاز جولجي ؛ ومع ذلك ، يتم تحديدها بواسطة غشاء ، مما يجعل كل صفيحة مستقلة عن الأخرى ، وتمتلك حبيبات وعضيات مختلفة السيتوبلازم و RNA.
كما هو متوقع ، فإن أبعاد الصفائح الدموية صغيرة بشكل خاص ؛ على الرغم من ذلك ، فإن بنيتها الداخلية معقدة للغاية ، لأنها تتدخل في عملية بيولوجية ذات أهمية أساسية تسمى تخثر الدم [هيماوالدم + ركود منع]. بالتآزر مع إنزيمات التخثر ، تسمح الصفائح الدموية بمرور الدم من السائل إلى الحالة الصلبة ، وتشكل نوعًا من السدادة (أو الجلطة) التي تسد النقاط المصابة من الأوعية.
القيم الطبيعية في الدم
عادة ما توجد 150.000 إلى 400.000 صفيحة في مليلتر واحد من الدم. متوسط عمرهم هو 10 أيام (مقارنة بـ 120 لكريات الدم الحمراء) ، وفي النهاية يتم بلعمهم أو تدميرهم بواسطة الضامة ، خاصة في الكبد والطحال (في الأخير يوجد ما يقرب من ثلث إجمالي كتلة الصفائح الدموية) يتم إنتاج 30.000 إلى 40.000 صفيحة لكل مم 3 يوميًا ؛ وإذا لزم الأمر ، يمكن أن يزيد هذا التخليق 8 مرات.
هيكل الصفائح الدموية
هيكل الصفائح الدموية معقد للغاية ، بحيث لا يتم تنشيطها إلا استجابة لمحفزات دقيقة ومحددة جيدًا ؛ إذا لم يكن الأمر كذلك ، فإن تراكم الصفائح الدموية في ظروف ليست ضرورية تمامًا ، أو عيبًا وقت الحاجة ، سيكون له عواقب وخيمة للغاية على الكائن الحي (تخثر الدم المرضي والنزيف).
نظرًا لأن تخثر الدم غير الصحيح يلعب دورًا ذا أهمية أساسية في نشأة السكتات الدماغية والنوبات القلبية ، فإن الآليات البيولوجية التي تتحكم فيه لا تزال موضوعًا للعديد من الدراسات.
توجد الصفائح الدموية دائمًا في الدورة الدموية ، ولكن لا يتم تنشيطها إلا عندما يكون هناك تلف في جدران الدورة الدموية.
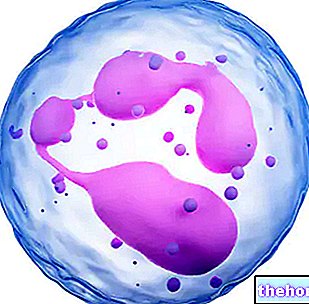
يتغير هيكل الصفائح الدموية ، وكذلك شكلها وحجمها ، بشكل عميق فيما يتعلق بدرجة ومرحلة النشاط. في الشكل غير النشط ، تتكون الصفائح الدموية من جزء شاحب (هيالومر) وجزء مركزي أكثر انكسارًا (كرومومير) ، غني بالحبيبات التي تحتوي على بروتينات التخثر والسيتوكينات. غشاء الخلية غني بجزيئات البروتين والبروتينات السكرية ، التي تعمل كمستقبلات من خلال تنظيم تفاعل الصفائح الدموية مع البيئة المحيطة (الالتصاق والتجمع).
التخثر والصفائح الدموية
الصفائح الدموية ليست سوى بعض من العديد من الجهات الفاعلة المشاركة في عملية التخثر. بعد إصابة أحد الأوعية الدموية ، فإن إطلاق بعض المواد الكيميائية بواسطة الخلايا البطانية ، والتعرض لكولاجين الجدار التالف ، يحددان تنشيط الصفائح الدموية (البطانة هي نسيج مبطّن خاص للسطح الداخلي للأوعية الدموية ، والتي في ظل الظروف العادية تفصل ألياف مصفوفة الكولاجين عن الدم مما يمنع التصاق الصفائح الدموية).
تلتصق الصفائح الدموية بسرعة بالكولاجين المكشوف في الجدار التالف (التصاق الصفائح الدموية) ويتم تنشيطها عن طريق إطلاق مواد معينة (تسمى السيتوكينات) في منطقة الآفة.هذه العوامل تعزز تنشيط وترابط الصفائح الدموية الأخرى ، والتي تتجمع لتشكيل سدادة هشة ، ما يسمى بالخثرة البيضاء ؛ علاوة على ذلك ، فهي تساعد على تقوية تضيق الأوعية المحلي الذي تسببه في السابق بعض المواد paracrine ، التي تطلقها البطانة المصابة بهدف تقليل تدفق الدم والضغط. يتم التوسط في كلا التفاعلين عن طريق إطلاق المواد الموجودة في بعض حبيبات الصفائح الدموية ، مثل السيروتونين والكالسيوم و ADP وعامل تنشيط الصفائح الدموية (PAF). يؤدي هذا الأخير إلى تشغيل مسار تأشير يحول فوسفوليبيدات غشاء الصفائح الدموية إلى ثرومبوكسان A2 ، والذي يحتوي على عمل مضيق للأوعية ويعزز تراكم الصفائح الدموية.
الصفائح الدموية هشة للغاية: بعد ثوان قليلة من إصابة الوعاء تتجمع وتتكسر ، وتطلق محتويات حبيباتها في الدم المحيط وتفضل تكوين جلطة.
من الواضح أن "تجمع الصفيحات" يجب أن يكون محدودًا لمنع سدادة الصفائح الدموية من الامتداد إلى مناطق لا تتأثر بالضرر البطاني ؛ وبالتالي ، فإن التصاق الصفائح الدموية بجدران الأوعية السليمة يكون مقيدًا بإفراز أكسيد النيتروجين والبروستاسكلين (إيكوسانويد).
يتم دمج سدادة الصفائح الدموية الأولية في المرحلة التالية ، حيث تتبع سلسلة من التفاعلات بعضها البعض بسرعة

بينما من ناحية ، فإن البروستاسكلين الذي تفرزه خلايا البطانة السليمة يمنع التصاق الصفائح الدموية ، من ناحية أخرى ، يصنع الجسم مضادات التخثر - مثل الهيبارين ومضاد الثرومبين III والبروتين C - لمنع وتنظيم بعض التفاعلات التي تنطوي عليها. شلال التخثر ، والذي يجب بالضرورة أن يقتصر على المنطقة المصابة.
مرحلة الأوعية الدموية ← تقليل تجويف الأوعية الدموية
تقلص عضلات الأوعية الدموية
تضيق الأوعية المحيطية
مرحلة الصفائح الدموية ← تشكيل سدادة الصفائح الدموية
عضوية
تغيير شكل
زوال الحبيبات
تجميع
مرحلة التخثر ← تكوين جلطة الفيبرين:
سلسلة من التفاعلات الأنزيمية
مرحلة الفبرينات ← انحلال الجلطة:
تفعيل نظام الفبرين
تلعب الصفائح الدموية دورًا أساسيًا في "إيقاف" النزيف ، لكنها لا تتدخل بشكل مباشر في إصلاح الوعاء الدموي التالف ، والذي يرجع بدلاً من ذلك إلى عمليات نمو الخلايا وانقسامها (الخلايا الليفية وخلايا العضلات الملساء الوعائية).بمجرد إصلاح التسرب ، تذوب الجلطة ببطء وتتراجع بفعل إنزيم البلازمين المحاصر داخل الجلطة.
البسترين واختبارات الدم
- PLT: عدد الصفائح الدموية ، عدد الصفائح الدموية لكل حجم دم
- MPV: متوسط حجم الصفائح الدموية
- PDW: عرض توزيع أحجام الصفائح الدموية (مؤشر تباين الصفائح الدموية)
- PCT: أو الهيماتوكريت الصفائح الدموية ، وهو حجم الدم الذي تحتله البسترينات




---ena-screening-o-pannello-ena.jpg)
-quando-preoccuparsi.jpg)






-e-bpco.jpg)









-cos-cause-sintomi-e-cura.jpg)
