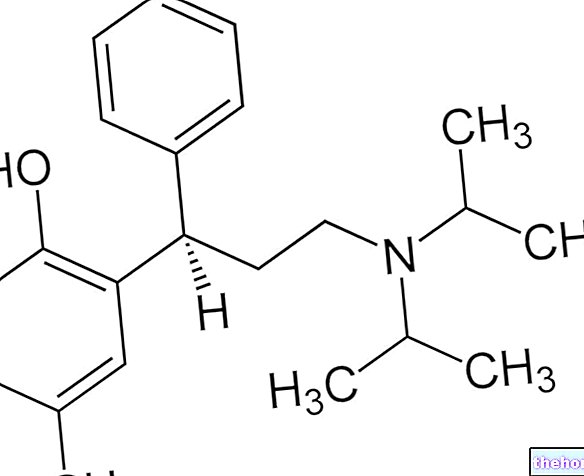
عام وتعريف
يتعامل علم التخلق مع دراسة كل تلك التعديلات الموروثة التي تؤدي إلى اختلافات في التعبير الجيني دون تغيير تسلسل الحمض النووي ، وبالتالي دون التسبب في تعديلات في تسلسل النيوكليوتيدات التي يتكون منها.

ومع ذلك ، باستخدام لغة أكثر تقنية ، يمكننا أن نؤكد أن علم التخلق يدرس كل تلك التعديلات وكل تلك التغييرات القادرة على تغيير النمط الظاهري للفرد ، دون تغيير النمط الجيني.
تُعزى ميزة "صياغة مصطلح" علم التخلق "إلى عالم الأحياء كونراد هال وادينجتون الذي عرَّفه في عام 1942 على أنه" فرع علم الأحياء الذي يدرس التفاعلات السببية بين الجينات ونواتجها ، ويؤدي إلى النمط الظاهري ".
شرح في هذه المصطلحات ، قد يبدو علم التخلق معقدًا إلى حد ما ؛ لفهم المفهوم بشكل أفضل ، قد يكون من المفيد فتح قوس صغير حول كيفية صنع الحمض النووي وكيف يتم نسخ الجينات التي يحتويها.
نسخ الحمض النووي والجينات
يوجد الحمض النووي داخل نواة الخلية ، وله بنية حلزونية مزدوجة ويتكون من وحدات متكررة تسمى نيوكليوتيدات.
يتم تنظيم معظم الحمض النووي الموجود داخل خلايانا في وحدات فرعية معينة تسمى nucleosomes.
تتكون النيوكليوسومات من جزء مركزي (يسمى النواة) يتكون من بروتينات تسمى الهستونات يلتف حولها الحمض النووي.
تشكل مجموعة الحمض النووي والهستونات ما يسمى بالكروماتين.
يعتمد نسخ الجينات الموجودة في الحمض النووي تحديدًا على "تغليف الأخير" داخل النيوكليوسومات. في الواقع ، يتم تنظيم عملية نسخ الجينات بواسطة عوامل النسخ ، والبروتينات الخاصة التي ترتبط بتسلسلات تنظيمية محددة موجودة على الحمض النووي والتي قادرة على تنشيط أو قمع - حسب الحالة - جينات معينة.
وبالتالي فإن الحمض النووي ذي المستوى المنخفض من التعبئة سيسمح لعوامل النسخ بالوصول إلى التسلسلات التنظيمية ، وعلى العكس من ذلك ، فإن الحمض النووي ذي المستوى العالي من التعبئة لن يسمح لهم بالوصول.
يتم تحديد مستوى التعبئة بواسطة الهستونات نفسها والتغييرات التي يمكن إجراؤها في تركيبها الكيميائي.
وبشكل أكثر تحديدًا ، فإن "أستلة الهستونات (أي إضافة مجموعة أسيتيل في مواقع معينة على الأحماض الأمينية التي تتكون منها هذه البروتينات) تجعل الكروماتين يفترض شكلاً" أكثر استرخاءً "يسمح بدخول عوامل النسخ ، وبالتالي نسخ الجينات من ناحية أخرى ، يزيل نزع الأسيتيل مجموعات الأسيتيل ، مما يتسبب في زيادة سمك الكروماتين وبالتالي منع النسخ الجيني.

الإشارات اللاجينية
في ضوء ما قيل حتى الآن ، يمكننا أن نؤكد أنه إذا قام علم التخلق بدراسة التعديلات القادرة على تغيير النمط الظاهري ، ولكن ليس النمط الجيني للفرد ، فإن الإشارة اللاجينية هي ذلك التعديل القادر على تغيير تعبير الجين المعين ، دون تغيير تسلسل النوكليوتيدات.
وبالتالي ، يمكننا أن نؤكد أن أستلة الهستونات المذكورة في الفقرة السابقة يمكن اعتبارها إشارة فوق جينية ؛ بمعنى آخر ، إنه تعديل جيني قادر على التأثير على نشاط الجين (الذي يمكن نسخه أو أقل) دون تغيير هيكلها.
نوع آخر من التعديل الوراثي اللاجيني يتكون من تفاعل المثيلة ، لكل من الحمض النووي والهستونات نفسها.
على سبيل المثال ، الميثيل (أي إضافة مجموعة ميثيل) للحمض النووي في موقع محفز يقلل من نسخ الجين ، الذي ينظم تنشيطه بواسطة موقع المروج نفسه. في الواقع ، موقع المحفز هو تسلسل محدد من الحمض النووي الموجود منبع الجينات ، وتتمثل مهمتها في السماح ببدء نسخ نفس الجينات. وبالتالي فإن إضافة مجموعة الميثيل في هذا الموقع تسبب نوعًا من العبء الذي يعيق النسخ الجيني.
ومع ذلك ، فإن الأمثلة الأخرى للتعديلات اللاجينية المعروفة حاليًا هي الفسفرة والتواجد في كل مكان.
يتم تنظيم كل هذه العمليات التي تتضمن الحمض النووي وبروتينات الهيستون (ولكن ليس فقط) بواسطة بروتينات أخرى يتم تصنيعها بعد نسخ الجينات الأخرى ، والتي يمكن بدورها تغيير نشاطها.
على أي حال ، فإن الميزة الأكثر إثارة للاهتمام في التعديل الوراثي اللاجيني هي أنه يمكن أن يحدث استجابة لمحفزات بيئية خارجية تتعلق ، على وجه التحديد ، بالبيئة المحيطة بنا ، وأسلوب حياتنا (بما في ذلك التغذية) وحالتنا الصحية.
بمعنى ما ، يمكن فهم التعديل اللاجيني على أنه تغيير تكيفي تديره الخلايا.
يمكن أن تكون هذه التغييرات فسيولوجية ، كما يحدث في حالة الخلايا العصبية التي تتبنى آليات جينية للتعلم والذاكرة ، ولكنها قد تكون أيضًا مرضية ، كما يحدث ، على سبيل المثال ، في حالة الاضطرابات العقلية أو الأورام.
الخصائص المهمة الأخرى للتعديلات اللاجينية هي القابلية للانعكاس والوراثة ، في الواقع ، يمكن أن تنتقل هذه التعديلات من خلية إلى أخرى ، على الرغم من أنها لا تزال تخضع لمزيد من التغييرات بمرور الوقت ، دائمًا استجابةً للمنبهات الخارجية.
أخيرًا ، يمكن أن تحدث التعديلات اللاجينية في مراحل مختلفة من الحياة وليس فقط على المستوى الجنيني (عندما تتمايز الخلايا) كما كان يُعتقد سابقًا ، ولكن أيضًا عندما يكون الكائن الحي قد تطور بالفعل.
الجوانب العلاجية
يمكن استغلال اكتشاف الوراثة اللاجينية والتعديلات اللاجينية على نطاق واسع في المجال العلاجي من أجل العلاج المحتمل لأنواع مختلفة من الأمراض ، بما في ذلك النوع الورمي (الأورام).
في الواقع ، كما ذكرنا ، يمكن أن تكون التعديلات اللاجينية ذات طبيعة مرضية ؛ لذلك ، في هذه الحالات ، يمكن تعريفها على أنها شذوذ حقيقي.
لذلك افترض الباحثون أنه إذا كان من الممكن أن تتأثر هذه التغييرات بمحفزات خارجية ويمكن أن تظهر نفسها وتعديل نفسها بشكل أكبر طوال حياة الكائن الحي ، فمن الممكن التدخل فيها باستخدام جزيئات محددة بهدف إعادة الوضع إلى الوضع الطبيعي. الظروف الطبيعية. هذا شيء لا يمكن فعله (على الأقل حتى الآن) عندما يكمن سبب المرض في طفرة جينية حقيقية.
لفهم هذا المفهوم بشكل أفضل ، يمكننا أن نأخذ كمثال على الاستخدام الذي استخدمه الباحثون لمعرفة علم التخلق في مجال العلاجات المضادة للسرطان.

-cos-cause-e-terapia.jpg)











fortuna-di-halloween.jpg)