المكونات النشطة: سيفيلامير (كربونات سيفيلامير)
رينفيلا 800 مجم أقراص مغلفة
تتوفر ملحقات عبوات Renvela لأحجام العبوات:- رينفيلا 800 مجم أقراص مغلفة
- Renvela 1.6g مسحوق للتعليق عن طريق الفم
- Renvela 2.4g مسحوق للتعليق الفموي
دواعي الإستعمال لماذا يتم استخدام رينفيلا؟ لما هذا؟
يحتوي الرينفيلا على المادة الفعالة sevelamer كربونات التي تعمل عن طريق منع امتصاص الفوسفات الموجود في الطعام في الجهاز الهضمي وبهذه الطريقة يقلل من مستويات الفوسفات في الدم.
يستخدم رينفيلا للسيطرة على فرط فوسفات الدم (مستويات عالية من الفوسفات في الدم) في:
- المرضى البالغين الذين يخضعون لغسيل الكلى (تقنية تصفية الدم). يمكن استخدام الدواء في المرضى الذين يخضعون لغسيل الكلى (باستخدام جهاز تنقية الدم) أو غسيل الكلى البريتوني (حيث يتم ضخ السوائل في البطن ويقوم غشاء داخلي للجسم بتصفية الدم) ؛
- مرضى أمراض الكلى المزمنة الذين لا يخضعون لغسيل الكلى ولديهم مستوى فوسفات في الدم يساوي أو يزيد عن 1.78 مليمول / لتر.
يجب استخدام رينفيلا مع علاجات أخرى ، مثل مكملات الكالسيوم وفيتامين د ، لمنع تطور أمراض العظام.
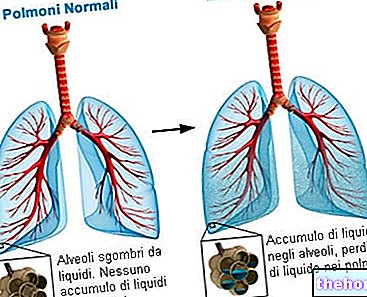
يمكن أن تؤدي زيادة مستويات الفوسفات في الدم إلى تكوين رواسب صلبة في الجسم تسمى التكلسات. ويمكن أن تؤدي هذه الترسبات إلى تصلب الأوعية الدموية وتجعل توزيع الدم في جميع أنحاء الجسم أكثر صعوبة. بالإضافة إلى ذلك ، يمكن أن تؤدي زيادة الفوسفات في الدم إلى حكة في الجلد واحمرار في العين وآلام العظام والكسور.
موانع الاستعمال عندما لا ينبغي استخدام رينفيلا
لا تأخذ رينفيلا
- إذا كان لديك مستويات منخفضة من الفوسفات في دمك (سيقوم طبيبك بفحصك).
- إذا كنت تعاني من انسداد معوي
- إذا كنت تعاني من حساسية تجاه المادة الفعالة أو أي من المكونات الأخرى لهذا الدواء (المدرجة في القسم 6).
احتياطات الاستخدام ما الذي تحتاج إلى معرفته قبل تناول رينفيلا
تحدث إلى طبيبك قبل تناول رينفيلا إذا كان أي مما يلي ينطبق عليك:
- مشاكل في البلع
- مشاكل في الحركة (الحركة) في المعدة والأمعاء
- قيء متكرر
- التهاب الأمعاء النشط
- خضع لعملية جراحية كبيرة في المعدة أو الأمعاء
الأطفال والمراهقون
لم يتم دراسة سلامة وفعالية الأطفال (أقل من 18 عامًا) ، لذلك لا ينصح باستخدام رينفيلا في الأطفال.
علاجات أخرى:
بسبب مرض الكلى أو علاج غسيل الكلى ، يمكنك:
- تعاني من انخفاض أو ارتفاع مستويات الكالسيوم في الدم. بما أن الرينفيلا لا يحتوي على الكالسيوم ، فقد يصف لك طبيبك مكملات الكالسيوم.
- لديهم مستوى منخفض من فيتامين د في الدم. نتيجة لذلك ، قد يفحص طبيبك مستويات فيتامين د في دمك ويصف فيتامين د إضافيًا حسب الحاجة. إذا كنت لا تتناول مكملات الفيتامينات المتعددة ، فقد يكون لديك أيضًا مستويات منخفضة من الفيتامينات A و E و K وحمض الفوليك في دمك ، وبالتالي قد يفحص طبيبك هذه المستويات ويصف مكملات الفيتامينات حسب الحاجة.
ملاحظة خاصة للمرضى الذين يخضعون لغسيل الكلى البريتوني:
قد يكون لديك التهاب الصفاق (عدوى سوائل البطن) المرتبط بغسيل الكلى الصفاقي. يمكن تقليل هذه المخاطر من خلال اعتماد تقنيات معقمة صارمة عند استبدال الأكياس. أخبر طبيبك على الفور إذا كنت تعاني من أي علامات أو أعراض جديدة لانزعاج في البطن ، أو تورم في البطن ، أو ألم في البطن ، أو ألم في البطن أو تصلب في البطن ، أو إمساك ، أو حمى ، أو قشعريرة ، أو غثيان أو قيء.
ستخضع لفحوصات أكثر دقة في حالة وجود مشاكل تتعلق بانخفاض مستويات الفيتامينات A و D و E و K وحمض الفوليك.
التفاعلات ما هي الأدوية أو الأطعمة التي قد تغير من تأثير رينفيلا
أخبر طبيبك إذا كنت تتناول أو تناولت مؤخرًا أو قد تتناول أي أدوية أخرى.
- لا ينبغي أن تؤخذ رينفيلا في وقت واحد مع سيبروفلوكساسين (مضاد حيوي).
- إذا كنت تتناول أدوية لمشاكل ضربات القلب أو الصرع ، فاستشر طبيبك عند تناول رينفيلا.
- قد تقلل رينفيلا من آثار الأدوية مثل السيكلوسبورين ، ميكوفينولات موفيتيل وتاكروليموس (الأدوية المستخدمة لتقليل نشاط الجهاز المناعي) سوف ينصحك طبيبك بما يجب عليك فعله إذا كنت تتناول هذه الأدوية.
- أدى الاستخدام المتزامن لليفوثيروكسين (دواء يستخدم لعلاج انخفاض مستويات هرمون الغدة الدرقية) ورينفيلا بشكل غير مألوف إلى نقص هرمون الغدة الدرقية لدى بعض المرضى ، ونتيجة لذلك ، يمكن للطبيب مراقبة مستويات هرمون الغدة الدرقية عن كثب في دمه.
- إذا كنت تتناول أدوية مثل أوميبرازول أو بانتوبرازول أو لانسوبرازول لعلاج حرقة المعدة أو مرض الجزر المعدي المريئي أو قرحة المعدة ، فاستشر طبيبك عند تناول رينفيلا.
سيتحقق طبيبك من أي تفاعلات بين رينفيلا والأدوية الأخرى على فترات منتظمة.
في بعض الحالات ، عندما يتعين تناول رينفيلا في نفس الوقت مع دواء آخر ، قد ينصحك طبيبك بتناول هذا الدواء قبل ساعة واحدة أو بعد 3 ساعات من تناول رينفيلا ، أو يفكر في فحص مستويات هذا الدواء في دمك.
تحذيرات من المهم معرفة ما يلي:
الحمل والرضاعة
إذا كنت حاملاً أو مرضعة ، تعتقدين أنك حامل أو تخططين لإنجاب طفل ، اسألي طبيبك للحصول على المشورة قبل تناول هذا الدواء. من غير المعروف ما إذا كان الرينفيلا يؤثر على الجنين.
أخبر طبيبك إذا كنت تريد إرضاع طفلك. من غير المعروف ما إذا كان رينفيلا يمكن أن يمر عبر حليب الثدي ويؤثر على الطفل.
السياقة واستعمال الماكنات
من غير المحتمل أن يؤثر رينفيلا على القدرة على القيادة أو استخدام الآلات.
الجرعة وطريقة ووقت الإدارة كيفية استخدام Renvela: Posology
يجب أن تتناول رينفيلا تمامًا كما أخبرك طبيبك. سيحدد طبيبك الجرعة على مستوى الفوسفات في الدم.
جرعة البدء الموصى بها من أقراص Renvela للبالغين وكبار السن (فوق 65 عامًا) هي حبة أو قرصين 800 مجم ، 3 مرات يوميًا مع الوجبات الرئيسية.
يجب ابتلاع الأقراص كاملة. لا سحق، مضغ، أو كسر أقراص.
سيقوم طبيبك في البداية بفحص مستويات الفوسفات في دمك كل 2-4 أسابيع وقد يقوم بتعديل جرعة رينفيلا ، إذا لزم الأمر ، للوصول إلى المستوى المناسب من الفوسفات.
يجب على المرضى الذين يتناولون رينفيلا الالتزام بالنظام الغذائي الموصوف.
إذا نسيت أن تأخذ رينفيلا
إذا فاتتك جرعة ، تناول الجرعة التالية في الوقت المعتاد مع الوجبة ، ولا تتناول جرعة مضاعفة لتعويض الجرعة المنسية.
الجرعة الزائدة ماذا تفعل إذا تناولت الكثير من الرينفيلا
في حالة الجرعة الزائدة المحتملة ، اتصل بطبيبك على الفور.
الآثار الجانبية ما هي الآثار الجانبية لرينفيلا
مثل جميع الأدوية ، يمكن أن يسبب هذا الدواء آثارًا جانبية ، على الرغم من عدم حدوثها لدى الجميع.
بما أن الإمساك يمكن أن يكون من الأعراض المبكرة لانسداد الأمعاء ، أخبر طبيبك أو الصيدلي.
تم الإبلاغ عن الآثار الجانبية التالية عند المرضى الذين يتناولون رينفيلا:
شائع جدًا (قد يؤثر على أكثر من 1 من كل 10 مستخدمين):
قيء ، إمساك ، ألم في الجزء العلوي من البطن ، غثيان.
شائعة (قد تؤثر على ما يصل إلى مستخدم واحد من بين كل 10 مستخدمين):
الإسهال وآلام البطن وعسر الهضم وانتفاخ البطن.
نادر جدًا (قد يؤثر على ما يصل إلى مستخدم واحد من بين 10000):
فرط الحساسية.
غير معروف (لا يمكن تقدير التردد من البيانات المتاحة):
كانت هناك تقارير عن حكة وطفح جلدي وبطء حركة الأمعاء (الحركة) / انسداد الأمعاء وانثقاب جدار الأمعاء.
التبليغ عن الأعراض الجانبية
إذا أصبت بأي أعراض جانبية ، تحدث إلى طبيبك ، بما في ذلك أي آثار جانبية محتملة غير مذكورة في هذه النشرة. يمكنك أيضًا الإبلاغ عن الآثار الجانبية مباشرةً عبر نظام الإبلاغ الوطني المدرج في الملحق الخامس. من خلال الإبلاغ عن الآثار الجانبية ، يمكنك المساعدة في توفير مزيد من المعلومات حول سلامة هذا الدواء.
انتهاء الصلاحية والاحتفاظ
احفظ هذا الدواء بعيدًا عن رؤية ومتناول أيدي الأطفال.
لا تستخدم هذا الدواء بعد تاريخ انتهاء الصلاحية المدون على الزجاجة والكرتون بعد "EXP".
احتفظ بالعبوة مغلقة بإحكام لحمايتها من الرطوبة.
لا يتطلب هذا الدواء أي شروط تخزين خاصة.
لا تقم بإلقاء أي أدوية في مياه الصرف الصحي أو النفايات المنزلية ، اسأل الصيدلي عن كيفية التخلص من الأدوية التي لم تعد تستخدمها ، فهذا سيساعد في حماية البيئة.
الموعد النهائي "> معلومات أخرى
ما يحتويه رينفيلا
- العنصر النشط هو كربونات سيفيلامير. يحتوي كل قرص مغلف من رينفيلا على 800 ملغ من كربونات سيفيلامير.
- المكونات الأخرى هي السليلوز الجريزوفولفين وكلوريد الصوديوم وستيرات الزنك. يحتوي طلاء القرص على هيدروميلوز (E464) وأحادي جليسريد ثنائي الأسيتيل. يحتوي حبر الطباعة على أكسيد الحديد الأسود (E172) ، وكحول الأيزوبروبيل ، والبروبيلين غليكول ، والهيبروميلوز (E464).
كيف يبدو رينفيلا وما هي محتويات العبوة
أقراص رينفيلا المغلفة هي أقراص بيضاء منقوشة على جانب واحد من RENVELA 800.
الأقراص معبأة في زجاجات بولي إيثيلين عالية الكثافة ، مزودة بغطاء من البولي بروبيلين وإغلاق بالحث.
التعبئة والتغليف:
- 1 × 30 حبة لكل زجاجة
- 1 × 180 حبة لكل زجاجة
- 180 حبة (6 عبوات بها 30 حبة)
قد لا يتم تسويق جميع أحجام العبوات.
نشرة حزمة المصدر: AIFA (وكالة الأدوية الإيطالية). تم نشر المحتوى في يناير 2016. المعلومات الموجودة قد لا تكون محدثة.
للوصول إلى أحدث إصدار ، يُنصح بالوصول إلى موقع AIFA (وكالة الأدوية الإيطالية). إخلاء المسؤولية والمعلومات المفيدة.
01.0 اسم المنتج الطبي -
رينفيل 800 ملغ أقراص مغلفة بالفيلم
02.0 التركيب النوعي والكمي -
يحتوي كل قرص على 800 مجم من كربونات سيفيلامير.
للحصول على قائمة كاملة من السواغات ، انظر القسم 6.1.
03.0 الشكل الصيدلاني -
قرص مغلف بالفيلم (قرص).
تم وضع علامة "RENVELA 800" على أحد الأجهزة اللوحية ذات اللون الأبيض إلى الأبيض الفاتح.
04.0 معلومات سريرية -
04.1 المؤشرات العلاجية -
يشار إلى Renvela للسيطرة على فرط فوسفات الدم في المرضى البالغين الذين يخضعون لغسيل الكلى أو غسيل الكلى البريتوني.
يشار إلى Renvela أيضًا في السيطرة على فرط فوسفات الدم لدى المرضى البالغين المصابين بأمراض الكلى المزمنة الذين لا يخضعون لغسيل الكلى باستخدام الفوسفور في الدم> 1.78 مليمول / لتر.
يجب استخدام الرينفيلا في سياق نهج متعدد العلاجات يمكن أن يشمل مكملات الكالسيوم ، 1،25-ديهيدروكسي-فيتامين د 3 أو أحد نظائرها للسيطرة على تطور أمراض العظام الكلوية.
04.2 الجرعة وطريقة الإدارة -
الجرعة
الجرعة الأولية
جرعة البدء الموصى بها لكربونات سيفيلامير هي 2.4 جرام أو 4.8 جرام يوميًا ، بناءً على الاحتياجات السريرية ومستويات الفوسفور في الدم. يجب تناول رينفيلا ثلاث مرات في اليوم مع وجبات الطعام.
* بالإضافة إلى المعايرة اللاحقة وفقًا للتعليمات
بالنسبة للمرضى الذين سبق لهم تناول مواد رابطة الفوسفات (سيفيلامير هيدروكلوريد أو الكالسيوم) ، يجب إعطاء رينفيلا بالجرام على أساس الجرام ، مع مراقبة مستويات الفوسفات لضمان الجرعات اليومية المثلى.
المعايرة والصيانة
يجب مراقبة مستويات الفوسفات ومعايرة جرعة كربونات سيفيلامير بزيادات قدرها 0.8 جم ثلاث مرات في اليوم (2.4 جم / يوم) كل 2-4 أسابيع حتى يتم الوصول إلى مستوى الفوسفور المصل المقبول ، تليها المراقبة المنتظمة.
يجب على المرضى الذين يتناولون رينفيلا الالتزام بالوجبات الغذائية الموصوفة.
في الممارسة السريرية ، سيكون العلاج مستمرًا ، بناءً على الحاجة إلى التحكم في مستويات الفوسفات ، وستكون الجرعة المتوقعة في المتوسط حوالي 6 جرام يوميًا.
سكان الأطفال
لم تثبت سلامة وفعالية رينفيلا لدى الأطفال دون سن 18 عامًا.
طريقة الإعطاء
استخدام عن طريق الفم.
يجب ابتلاع الأقراص كاملة ولا يجب سحقها أو مضغها أو سحقها قبل الإعطاء
04.3 موانع -
• فرط الحساسية للمادة الفعالة أو لأي من السواغات المدرجة في القسم 6.1.
• نقص فوسفات الدم
• انسداد الأمعاء.
04.4 تحذيرات خاصة واحتياطات مناسبة للاستخدام -
لم تثبت سلامة وفعالية رينفيلا لدى المرضى البالغين المصابين بأمراض الكلى المزمنة ولا يخضعون لغسيل الكلى بفوسفور المصل.
لم يتم إثبات سلامة وفعالية رينفيلا في المرضى الذين يعانون من الاضطرابات التالية:
• عسر البلع
• اضطرابات البلع
• اضطرابات حركية الجهاز الهضمي الشديدة بما في ذلك خزل المعدة الشديد أو غير المعالج ، واحتباس محتويات المعدة وحركة الأمعاء غير الطبيعية أو غير المنتظمة
• مرض التهاب الأمعاء النشط
• جراحة كبرى في الجهاز الهضمي
لذلك ، يجب توخي الحذر عند استخدام رينفيلا لدى هؤلاء المرضى.
انسداد معوي والعلوص / تحت القناة
في حالات نادرة جدًا ، لوحظ انسداد الأمعاء والعلاق / الجزء السفلي في المرضى أثناء العلاج باستخدام sevelamer hydrochloride (كبسولات / أقراص) ، والذي يحتوي على نفس الجزء النشط مثل كربونات sevelamer. يمكن أن يكون الإمساك نذير. يجب مراقبة المرضى الذين يعانون من الإمساك عن كثب أثناء علاج رينفيلا. يجب إعادة تقييم علاج رينفيلا في المرضى الذين يعانون من إمساك شديد أو أعراض معدية معوية شديدة أخرى.
الفيتامينات التي تذوب في الدهون
مرضى الكلى المزمن (فشل كلوي مزمن، مرض الكلى المزمن) قد يُظهر نقصًا في الفيتامينات القابلة للذوبان في الدهون A و D و E و K ، اعتمادًا على النظام الغذائي وشدة المرض. لا يمكن استبعاد أن الرينفيلا قد ترتبط بالفيتامينات التي تذوب في الدهون الموجودة في الأطعمة المبتلعة. يجب تقييم مستويات الفيتامينات A و D و E و K في المصل على فترات منتظمة عند المرضى الذين يتناولون سيفيلامير ولكن بدون مكملات الفيتامينات ، ويوصى باستخدام مكملات الفيتامينات عند الضرورة. يوصى باستخدام مكملات فيتامين د (حوالي 400 وحدة دولية من فيتامين د الأصلي يوميًا) لمرضى الكلى المزمن الذين لا يخضعون لغسيل الكلى ، والتي قد تكون جزءًا من مستحضر متعدد الفيتامينات يتم تناوله بعيدًا عن جرعة رينفيلا. في المرضى الذين يخضعون لغسيل الكلى البريتوني ، يوصى بمراقبة إضافية للفيتامينات التي تذوب في الدهون وحمض الفوليك ، حيث لم يتم قياس مستويات فيتامين أ ، د ، هـ ، ك في دراسة سريرية لهؤلاء المرضى.
نقص حمض الفوليك
لا توجد حاليًا بيانات كافية لاستبعاد احتمال نقص حمض الفوليك أثناء العلاج طويل الأمد مع رينفيلا.
نقص كالسيوم الدم / فرط كالسيوم الدم
يمكن للمرضى المصابين بمرض الكلى المزمن أن يصابوا بنقص كالسيوم الدم أو فرط كالسيوم الدم. رينفيلا لا يحتوي على الكالسيوم. وبالتالي ، يجب مراقبة مستويات الكالسيوم في الدم على فترات منتظمة وإعطاء مكمل الكالسيوم الأساسي إذا لزم الأمر.
الحماض الأيضي
المرضى الذين يعانون من أمراض الكلى المزمنة معرضون لـ "الحماض الاستقلابي. لذلك يوصى بمراقبة مستويات بيكربونات المصل كجزء من الممارسة السريرية الجيدة".
التهاب الصفاق
يخضع مرضى غسيل الكلى لبعض مخاطر الإصابة المتأصلة في طريقة غسيل الكلى المحددة. التهاب الصفاق هو أحد المضاعفات المعروفة لدى المرضى الذين يخضعون لغسيل الكلى الصفاقي ، وقد تم الإبلاغ عن المزيد من حالات التهاب الصفاق في مجموعة سيفيلامير مقارنة بمجموعة التحكم في دراسة سريرية لسيفيلامير هيدروكلوريد. يجب متابعة المرضى الذين يتلقون غسيل الكلى الصفاقي عن كثب لضمان استخدام تقنية التعقيم الصحيحة وتحديد وإدارة أي علامات وأعراض مرتبطة بالتهاب الصفاق في الوقت المناسب.
صعوبة في البلع والاختناق
تم الإبلاغ عن صعوبة في ابتلاع أقراص Renvela بشكل نادر. تضمنت العديد من هذه الحالات مرضى يعانون من حالات مرضية مصاحبة ، بما في ذلك اضطرابات البلع أو تشوهات المريء. لذلك ، يجب توخي الحذر عند إعطاء رينفيلا للمرضى الذين يعانون من صعوبات في البلع. يجب استخدام مسحوق Renvela للتعليق الفموي للمرضى الذين لديهم تاريخ من صعوبات في البلع.
قصور الغدة الدرقية
يوصى بمراقبة المرضى الذين يعانون من قصور الغدة الدرقية بشكل مشترك مع كربونات سيفيلامير وليفوثيروكسين (انظر القسم 4.5).
علاج مزمن طويل الأمد
لم يكن هناك دليل على تراكم sevelamer من دراسة سريرية لمدة عام واحد. ومع ذلك ، لا يمكن استبعاد احتمال امتصاص وتراكم سيفيلامير في العلاج المزمن طويل الأمد (> سنة واحدة) (انظر القسم 5.2).
بفرط نشاط جارات الدرق
رينفيلا غير محدد للسيطرة على فرط نشاط جارات الدرق.في المرضى الذين يعانون من فرط نشاط جارات الدرق الثانوي ، يجب استخدام رينفيلا في سياق نهج متعدد العلاجات ، والذي قد يشمل مكملات الكالسيوم ، 1،25-ديهيدروكسي-فيتامين د 3 أو أحد نظائرها ، لتقليل مستويات هرمون الغدة الجار درقية (iPTH) سليمة.
04.5 التفاعلات مع المنتجات الطبية الأخرى وأشكال التفاعل الأخرى -
غسيل الكلى
لم يتم إجراء دراسات تفاعل في مرضى غسيل الكلى.
سيبروفلوكساسين
في دراسات التفاعل على متطوعين أصحاء ، sevelamer hydrochloride ، الذي يحتوي على نفس الجزء النشط مثل Renvela ، قلل من التوافر البيولوجي للسيبروفلوكساسين بحوالي 50٪ مع الإعطاء المتزامن لـ sevelamer hydrochloride في دراسة جرعة واحدة. وبالتالي ، لا ينبغي تناول Renvela في نفس الوقت مثل سيبروفلوكساسين.
سيكلوسبورين ، ميكوفينولات موفيتيل وتاكروليموس في مرضى الزرع
تم الإبلاغ عن انخفاض مستويات السيكلوسبورين و mycophenolate mofetil و tacrolimus في متلقي الزرع ، مع ما يصاحب ذلك من تعاطي مع sevelamer hydrochloride ، دون عواقب إكلينيكية (مثل رفض الزرع). لا يمكن استبعاد التفاعلات ، لذلك يجب مراعاة المراقبة الدقيقة لتركيزات السيكلوسبورين والميكوفينولات موفيتيل والتاكروليموس في الدم أثناء استخدام المجموعة وبعد إيقافها.
ليفوثيروكسين
تم الإبلاغ عن حالات نادرة جدًا من قصور الغدة الدرقية في المرضى الذين يعانون من تناول ما يصاحب ذلك من هيدروكلوريد سيفيلامير ، والذي يحتوي على نفس الجزء النشط مثل كربونات سيفيلامير وليفوثيروكسين. لذلك ، يوصى بالمراقبة الدقيقة لمستويات هرمون الغدة الدرقية (TSH) في المرضى الذين يتلقون كربونات سيفيلامير وليفوثيروكسين.
الأدوية المضادة للجروح ومضادات الاختلاج
تم استبعاد المرضى الذين يتناولون مضادات اضطراب النظم للسيطرة على عدم انتظام ضربات القلب ومضادات الاختلاج للسيطرة على اضطرابات النوبات من التجارب السريرية. يجب توخي الحذر عند وصف رينفيلا للمرضى الذين يتناولون هذه المنتجات الطبية أيضًا.
ديجوكسين أو وارفارين أو إنالابريل أو ميتوبرولول
في دراسات التفاعل التي أجريت على متطوعين أصحاء ، لم يكن لسيفيلامير هيدروكلوريد ، الذي يحتوي على نفس الجزء النشط مثل كربونات سيفيلامير ، أي تأثير على التوافر البيولوجي للديجوكسين أو الوارفارين أو إنالابريل أو ميتوبرولول.
التوافر البيولوجي
الرينفيلا لا يمتص وقد يؤثر على التوافر البيولوجي للمنتجات الطبية الأخرى. عند إدارة أي منتج طبي ، حيث يكون لأي انخفاض في التوافر البيولوجي تأثير مهم سريريًا على السلامة أو الفعالية ، يجب إعطاء المنتج الطبي قبل ساعة واحدة على الأقل ، أو بعد ثلاث ساعات على الأقل من تناول رينفيلا. بدلاً من ذلك ، يجب أن يفكر الطبيب في فحص مستويات الدم.
04.6 الحمل والرضاعة:
حمل
لا توجد بيانات أو بيانات محدودة من استخدام sevelamer في النساء الحوامل. أظهرت الدراسات التي أجريت على الحيوانات سمية إنجابية مع إعطاء sevelamer بجرعات عالية في الجرذان (انظر القسم 5.3). وقد ثبت أيضًا أن sevelamer يقلل من امتصاص العديد من الفيتامينات ، بما في ذلك حمض الفوليك (انظر القسمين 4.4 و 5.3). المخاطر المحتملة على البشر غير معروفة. يجب إعطاء Renvela فقط للنساء الحوامل إذا كانت هناك حاجة ماسة إليها وبعد "تحليل دقيق لنسبة المخاطر / الفائدة لكل من الأم والأم الجنين.
وقت الأكل
من غير المعروف ما إذا كان سيفيلامير / مستقلبات يتم إفرازها في حليب الثدي البشري. حقيقة أن سيفيلامير لا يمتص يجعل إفرازه في حليب الثدي أمرًا غير محتمل. يجب اتخاذ قرار بمواصلة / التوقف عن الرضاعة الطبيعية أو الاستمرار / التوقف عن علاج رينفيلا مع الأخذ في الاعتبار فائدة الرضاعة الطبيعية للطفل وفائدة علاج رينفيلا للمرأة.
خصوبة
لا توجد بيانات عن تأثير sevelamer على خصوبة الإنسان. أظهرت الدراسات التي أجريت على الحيوانات أن سيفيلامير لم يؤثر على الخصوبة لدى ذكور وإناث الجرذان عند التعرض لجرعة مكافئة للإنسان ضعف جرعة التجربة السريرية القصوى البالغة 13 جم / يوم بناءً على مقارنة مساحة سطح الجسم النسبية.
04.7 التأثيرات على القدرة على القيادة واستخدام الآلات -
Sevelamer ليس له تأثير أو تأثير ضئيل على القدرة على القيادة أو استخدام الآلات.
04.8 الآثار غير المرغوب فيها -
ملخص ملف تعريف السلامة
التفاعلات الضائرة الأكثر شيوعًا (> 5٪ من المرضى) تقع جميعها في اضطرابات الجهاز الهضمي حسب فئة أعضاء النظام. كانت معظم هذه التفاعلات الضائرة خفيفة إلى معتدلة الشدة.
جدول التفاعلات العكسية
تم فحص سلامة sevelamer (مثل أملاح الكربونات وهيدروكلوريد) في العديد من الدراسات السريرية التي شملت ما مجموعه 969 مريضًا يخضعون لغسيل الكلى ، مع علاجات تستمر من 4 إلى 50 أسبوعًا (724 مريضًا تم علاجهم باستخدام sevelamer hydrochloride و 245 مريضًا باستخدام كربونات sevelamer) ، 97 مرضى غسيل الكلى البريتوني الذين عولجوا لمدة 12 أسبوعًا (جميعهم عولجوا باستخدام سيفيلامير هيدروكلوريد) و 128 مريضًا مصابًا بمرض الكلى المزمن غير الكلوي في العلاج لمدة 8-12 أسبوعًا (علاج 79 مريضًا باستخدام سيفيلامير هيدروكلوريد و 49 مريضًا بكربونات سيفيلامير).
يتم سرد التفاعلات العكسية حسب التردد في الجدول أدناه. يُصنف تواتر التقارير على أنه شائع جدًا (> 1/10) ، شائع (> 1/100 ، 1/1000 ، 1/10000 ،
الإبلاغ عن ردود الفعل السلبية المشتبه بها
يعد الإبلاغ عن التفاعلات العكسية المشتبه بها التي تحدث بعد ترخيص المنتج الطبي أمرًا مهمًا لأنه يسمح بالمراقبة المستمرة لتوازن الفوائد / المخاطر للمنتج الطبي. يُطلب من المتخصصين في الرعاية الصحية الإبلاغ عن أي ردود فعل سلبية مشتبه بها عبر نظام الإبلاغ الوطني. في "الملحق الخامس" .
04.9 جرعة زائدة -
تم إعطاء Sevelamer hydrochloride ، الذي يحتوي على نفس الجزء النشط مثل كربونات sevelamer ، لمتطوعين أصحاء عاديين بجرعات تصل إلى 14 جرامًا / يوم لمدة ثمانية أيام ، دون التسبب في آثار غير مرغوب فيها. في المرضى الذين يعانون من مرض الكلى المزمن ، كانت الجرعة اليومية القصوى التي تمت دراستها في المتوسط 14.4 جرامًا من كربونات سيفيلامير في جرعة يومية واحدة.
05.0 الخصائص الصيدلانية -
05.1 "الخصائص الديناميكية الدوائية -
الفصيلة العلاجية: علاج فرط فوسفات الدم.
كود ATC: V03A E02.
يحتوي الرينفيلا على سيفيلامير ، وهو بوليمر غير قابل للامتصاص ومخلب للفوسفات وخالٍ من المعدن أو الكالسيوم. يحتوي Sevelamer على العديد من الأمينات المفصولة من خلال الكربون من البنية الأساسية للبوليمر ، والتي تتحول إلى بروتونات في المعدة. ترتبط هذه الأمينات البروتونية سلبًا بالأيونات المشحونة ، مثل الفوسفات الغذائي ، في الأمعاء. من خلال ربط الفوسفات في الأمعاء وتخفيف امتصاصه ، يقلل sevelamer تركيز الفوسفور في الدم ، والرصد المنتظم لمستويات الفوسفات ضروري دائمًا أثناء إعطاء مواد رابطة الفوسفات.
في تجربتين سريريتين عشوائيتين متقاطعتين ، تبين أن كربونات سيفيلامير ، في كل من تركيبات الأقراص والمسحوق ، مكافئة علاجيًا لـ sevelamer hydrochloride عند إعطائها ثلاث مرات في اليوم ، وبالتالي فهي فعالة في السيطرة على فوسفات الدم لدى المرضى. مع CKD يخضع لغسيل الكلى.
أظهرت الدراسة الأولى أن تناول كربونات sevelamer ثلاث مرات / يوم كان مكافئًا لأقراص sevelamer hydrochloride ثلاث مرات / يوم في 79 مريضًا من مرضى غسيل الكلى تم علاجهم على مدى فترتين من العلاج العشوائي لمدة 8 أسابيع (بمتوسطات مرجحة للوقت متوسط فوسفات المصل يساوي 1.5 ± 0.3 ملي مول). / لتر لكل من كربونات سيفيلامير وهيدروكلوريد سيفيلامير). أظهرت الدراسة الثانية التكافؤ بين مسحوق كربونات sevelamer ، الذي يتم تناوله ثلاث مرات يوميًا ، وأقراص sevelamer hydrochloride التي تُعطى ثلاث مرات يوميًا إلى 31 مريضًا يعانون من غسيل الكلى المصابين بفرط فوسفات الدم (يُعرف بمستويات فوسفات المصل> 1.78 مليمول / لتر) ، في "فترة من 4 إلى 4. فترات العلاج العشوائية في الأسبوع (بمتوسط فوسفات مصل مرجح بالوقت يبلغ 1.6 ± 0.5 مليمول / لتر لمسحوق كربونات سيفيلامير ، و 1.7 ± 0.4 مليمول / لتر لأقراص سيفيلامير هيدروكلوريد).
في الدراسات السريرية التي أجريت على مرضى غسيل الكلى ، لم يُظهر سيفيلامير وحده تأثيرًا ثابتًا وهامًا سريريًا على مستويات هرمون الغدة الجار درقية (iPTH) في المصل. في دراسة استمرت 12 أسبوعًا على المرضى الذين يخضعون لغسيل الكلى البريتوني ، لوحظ انخفاض في iPTH مماثل لتلك الخاصة بالمرضى الذين يتلقون أسيتات الكالسيوم. في المرضى الذين يعانون من فرط نشاط جارات الدرق الثانوي ، يجب استخدام Renvela في سياق نهج علاجي متعدد ، والذي يمكن أن يشمل الكالسيوم كمكملات ، أو 1،25-dihydroxy-Vitamin D3 أو أحد نظائرها ، لتقليل هرمون الغدة الجار درقية (iPTH).
تم إثبات ارتباط sevelamer بالأحماض الصفراوية في المختبر و في الجسم الحي، ضمن نماذج الحيوانات التجريبية. ربط حمض الصفراء براتنجات التبادل الأيوني هو طريقة مثبتة لخفض نسبة الكوليسترول في الدم.في الدراسات السريرية على سيفيلامير ، انخفض كل من متوسط الكوليسترول الكلي وكوليسترول LDL بنسبة 15- 39٪. لوحظ انخفاض في الكوليسترول بعد 2 أسابيع من العلاج ويتم الحفاظ عليها بعلاج طويل الأمد لم تتغير الدهون الثلاثية وكوليسترول البروتين الدهني عالي الكثافة والألبومين بعد العلاج باستخدام سيفيلامير.
نظرًا لأن sevelamer يربط الأحماض الصفراوية ، فقد يتداخل مع امتصاص الفيتامينات التي تذوب في الدهون مثل الفيتامينات A و D و E و K.
لا يحتوي Sevelamer على الكالسيوم ويقلل من حدوث نوبات فرط كالسيوم الدم ، مقارنةً بالمرضى الذين يتناولون مواد رابطة الفوسفات التي تحتوي على الكالسيوم فقط. وقد ثبت أن تأثير sevelamer على الفوسفور والكالسيوم قد تم الحفاظ عليه طوال مدة دراسة المتابعة. لمدة سنة واحدة تم الحصول على هذه المعلومات من الدراسات التي تم فيها استخدام هيدروكلوريد سيفيلامير.
05.2 "خصائص حركية الدواء -
لم يتم إجراء دراسات حركية الدواء على كربونات سيفيلامير. لا يتم امتصاص Sevelamer hydrochloride ، الذي يحتوي على نفس الجزء النشط مثل كربونات sevelamer ، من الجهاز الهضمي ، كما أكدت دراسة الامتصاص في متطوعين أصحاء.
05.3 بيانات السلامة قبل السريرية -
لا تكشف البيانات غير الإكلينيكية عن سيفيلامير أي خطر خاص على البشر بناءً على الدراسات التقليدية لعلم الأدوية الآمن أو السمية المتكررة للجرعات أو السمية الجينية.
أجريت دراسات السرطنة باستخدام هيدروكلوريد سيفيلامير الفموي في الفئران (جرعات تصل إلى 9 جم / كجم / يوم) والجرذان (0.3 ، 1 أو 3 جم / كجم / يوم). كان هناك "زيادة في حدوث الورم الحليمي الخلوي العابر للمثانة البولية في ذكور الجرذان ، في مجموعة الجرعات العالية (الجرعة البشرية تعادل ضعف جرعة التجربة السريرية القصوى البالغة 14.4 جم). لم يكن هناك زيادة في الإصابة. الأورام في الفئران ( الجرعة البشرية المكافئة تضاعف ثلاثة أضعاف الجرعة القصوى في الدراسات السريرية).
في اختبار وراثي خلوي في المختبر في الثدييات ، مع التنشيط الأيضي ، تسبب sevelamer hydrochloride في زيادة ذات دلالة إحصائية في عدد الانحرافات الهيكلية للكروموسومات. لم يكن هيدروكلوريد سيفيلامير مطفراً في مقايسة الطفرة البكتيرية أميس.
في الجرذان والكلاب ، قلل sevelamer من امتصاص الفيتامينات القابلة للذوبان في الدهون D و E و K (عوامل التخثر) وحمض الفوليك.
لوحظ وجود عجز في تعظم الهيكل العظمي في مواقع مختلفة في أجنة إناث الجرذان التي تلقت سيفيلامير بجرعات متوسطة وعالية (جرعة بشرية مكافئة أقل من الحد الأقصى لجرعة التجربة السريرية البالغة 14.4 جم) وقد تكون هذه التأثيرات ثانوية لنضوب فيتامين د
في الأرانب الحوامل الذين تلقوا جرعات فموية من sevelamer hydrochloride مع gavage ، كانت هناك زيادة في الارتشاف المبكر في مجموعة الجرعات العالية أثناء تكوين الأعضاء (الجرعة البشرية المكافئة ضعف الجرعة القصوى في مجموعة الجرعات العالية). الدراسات السريرية).
لم يؤثر Sevelamer hydrochloride على خصوبة الذكور أو الإناث في الجرذان في دراسة الإدارة الغذائية حيث عولجت الإناث من 14 يومًا قبل التزاوج إلى الحمل ، والذكور لمدة 28 يومًا قبل الحمل.كانت الجرعة القصوى في هذه الدراسة بالذات 4.5 جم / كجم / يوم (الجرعة البشرية المكافئة ضعف الجرعة القصوى في الدراسات السريرية البالغة 13 جم / يوم ، بناءً على مقارنة مساحة سطح الجسم النسبية).
06.0 معلومات صيدلانية -
06.1 سواغ -
لوح:
السليلوز الجريزوفولفين
كلوريد الصوديوم
ستيرات الزنك
فيلم طلاء:
هيبروميلوز (E464)
أحادي الجليسريد ثنائي الأسيتيل
حبر الطباعة:
أكسيد الحديد الأسود (E172)
البروبيلين غليكول
ايزوبروبيل
هيبروميلوز (E464)
06.2 عدم التوافق "-
غير ذات صلة.
06.3 فترة الصلاحية "-
3 سنوات.
06.4 احتياطات خاصة للتخزين -
احتفظ بالزجاجة مغلقة بإحكام لحماية الدواء من الرطوبة.
لا يتطلب هذا المنتج الطبي أي درجات حرارة تخزين خاصة.
06.5 طبيعة العبوة الفورية ومحتويات العبوة -
زجاجات HDPE مزودة بغطاء بولي بروبيلين وإغلاق بالحث من الألومنيوم.
تحتوي كل عبوة على 30 قرصاً أو 180 قرصاً.
عبوات تحتوي على 30 أو 180 قرصًا وحزمة متعددة تحتوي على 180 (6 عبوات بها 30 قرصًا).
قد لا يتم تسويق جميع أحجام العبوات.
06.6 تعليمات الاستخدام والتعامل -
يجب التخلص من الأدوية غير المستخدمة والنفايات الناتجة عن هذا الدواء وفقًا للوائح المحلية.
07.0 حائز على "ترخيص التسويق" -
Genzyme Europe B.V.
Gooimeer 10
1411 DD Naarden
هولندا
08.0 رقم ترخيص التسويق -
EU / 1/09/521/001
039480013
EU / 1/09/521/002
039480025
EU / 1/09/521/003
039480037
09.0 تاريخ أول تفويض أو تجديد التفويض -
تاريخ الترخيص الأول: 10 يونيو 2009
10.0 تاريخ مراجعة النص -
مارس 2014