المكونات النشطة: باليفيزوماب
Synagis 50 mg مسحوق ومذيب لمحلول الحقن.
دواعي الإستعمال لماذا يتم استخدام Synagis؟ لما هذا؟
يحتوي Synagis على مادة فعالة تسمى palivizumab ، وهو جسم مضاد يعمل بشكل خاص ضد فيروس يسمى الفيروس المخلوي التنفسي RSV.
يتعرض الطفل لخطر كبير للإصابة بالمرض الناجم عن فيروس يسمى الفيروس المخلوي التنفسي (RSV).
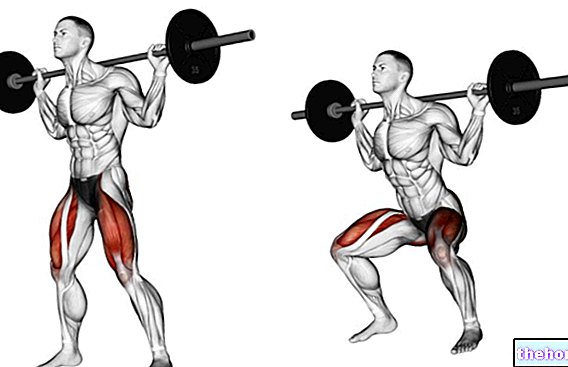
الأطفال الأكثر عرضة للإصابة بمرض RSV الشديد (الأطفال المعرضون لخطر كبير) هم أطفال يولدون قبل الأوان (35 أسبوعًا أو أقل) أو أطفال يولدون بمشاكل معينة في القلب أو الرئة.
Synagis هو دواء يساعد على حماية طفلك من الإصابة بمرض RSV الشديد.
موانع عندما لا ينبغي استخدام Synagis
لا تستخدم Synagis في الطفل
إذا كنت تعاني من حساسية تجاه عقار باليفيزوماب أو أي من المكونات الأخرى لهذا الدواء المدرجة في القسم 6.
يمكن أن تشمل علامات وأعراض رد الفعل التحسسي الشديد ما يلي:
- طفح جلدي شديد ، وخلايا النحل ، وحكة في الجلد
- تورم في الشفتين أو اللسان أو الوجه
- انسداد الحلق وصعوبة البلع
- التنفس الصعب أو السريع أو غير المنتظم
- زرقة الجلد أو الشفتين أو تحت الأظافر
- ضعف أو ارتخاء العضلات
- انخفاض ضغط الدم
- عدم الاستجابة
احتياطات للاستخدام ما تحتاج إلى معرفته قبل تناول سيناجيس
توخ الحذر مع Synagis
- إذا شعر الطفل بتوعك. يرجى إخبار طبيبك إذا كان طفلك يشعر بتوعك ، لأن إدارة Synagis قد تحتاج إلى تأخير.
- إذا كان الطفل يعاني من مظاهر نزفية ، حيث يتم عادة حقن Synagis في الفخذ.
التفاعلات الأدوية أو الأطعمة التي قد تغير من تأثير سيناجيس
لا توجد تفاعلات معروفة لـ Synagis مع أدوية أخرى. ومع ذلك ، قبل البدء في علاج Synagis ، يجب أن تخبر طبيبك عن جميع الأدوية التي يتناولها طفلك حاليًا.
الجرعة وطريقة الاستخدام كيفية استخدام Synagis: الجرعة
كم مرة يجب إعطاء Synagis للطفل؟
يجب إعطاء Synagis للطفل بجرعة 15 مجم / كجم من وزن الجسم مرة واحدة في الشهر طالما استمر خطر الإصابة بفيروس RSV. لحماية الطفل بشكل أفضل ، يجب عليك اتباع تعليمات طبيبك بشأن موعد العودة لجرعات إضافية من Synagis.
إذا كان الطفل قد خضع لعملية جراحية في القلب (جراحة المجازة القلبية) ، فقد يحتاج إلى جرعة إضافية من Synagis بعد الجراحة ، وبعد ذلك ، يمكن للطفل استئناف جدول الحقن الأصلي.
كيف يتلقى الطفل سيناجيس؟
سيتم إعطاء Synagis لطفلك عن طريق الحقن في العضلات ، عادة في الفخذ الخارجي.
ماذا يحدث عندما يفوت الطفل حقنة Synagis؟
إذا فات طفلك حقنة ، يجب عليك الاتصال بطبيبك في أقرب وقت ممكن.كل حقنة من Synagis تحمي طفلك لمدة شهر تقريبًا قبل الحاجة إلى حقنة أخرى.
استخدم هذا الدواء دائمًا تمامًا كما أخبرك طبيبك أو الصيدلي. إذا كان لديك أي أسئلة أخرى حول استخدام هذا الدواء ، اسأل طبيبك أو الصيدلي
الآثار الجانبية ما هي الآثار الجانبية ل Synagis
مثل جميع الأدوية ، يمكن أن يسبب هذا الدواء آثارًا جانبية ، على الرغم من عدم حدوثها لدى الجميع.
يمكن أن يسبب Synagis آثارًا جانبية خطيرة بما في ذلك:
- ردود الفعل التحسسية الشديدة ، يمكن أن تكون هذه التفاعلات مهددة للحياة أو قاتلة (انظر "لا تستخدم سيناجيس في طفلك" للحصول على قائمة بالعلامات والأعراض).
- كدمات غير عادية أو مجموعات من البقع الحمراء الصغيرة على الجلد.
أخبر طبيبك أو اطلب المساعدة الطبية على الفور إذا كان طفلك يعاني من أي من الآثار الجانبية الخطيرة المذكورة أعلاه بعد تلقي جرعة من Synagis.
أعراض جانبية أخرى
شائع جدًا (يصيب شخصًا واحدًا على الأقل من كل 10 أشخاص):
- متسرع
- حمى
شائع (يصيب 1 إلى 10 مستخدمين في 100):
- ألم أو احمرار أو تورم في موقع الحقن
- توقف في التنفس أو صعوبات أخرى في التنفس
غير شائع (يصيب أقل من 1 من كل 100 شخص):
- تشنجات
- الشرى
التبليغ عن الأعراض الجانبية
إذا أصيب طفلك بأي آثار جانبية ، يرجى الاتصال بطبيبك. يتضمن ذلك أي آثار جانبية محتملة غير مذكورة في هذه النشرة. يمكنك أيضًا الإبلاغ عن الآثار الجانبية مباشرةً عبر نظام الإبلاغ الوطني المدرج في الملحق الخامس. من خلال الإبلاغ عن الآثار الجانبية ، يمكنك المساعدة في توفير مزيد من المعلومات حول سلامة هذا الدواء.
انتهاء الصلاحية والاحتفاظ
احفظ هذا الدواء بعيدًا عن رؤية ومتناول أيدي الأطفال.
لا تستخدم هذا الدواء بعد تاريخ انتهاء الصلاحية المدون على الملصق.
يحفظ في الثلاجة (2 درجة مئوية - 8 درجة مئوية).
استخدم في غضون 3 ساعات من إعادة التركيب.
لا تجمد.
احفظ القارورة في الكرتون الخارجي لحمايتها من الضوء.
معلومات أخرى
ما يحتويه Synagis
- العنصر النشط هو palivizumab. 50 مجم لكل قارورة ، والتي توفر 100 مجم / مل من باليفيزوماب عند إعادة تركيبها وفقًا للإرشادات.
- المكونات الأخرى هي:
- للمسحوق: الهيستيدين والجليسين والمانيتول.
- للمذيب: ماء للحقن.
كيف يبدو Synagis وما هي محتويات العبوة
يأتي Synagis على شكل مسحوق ومذيب للحقن (50 مجم من المسحوق في قنينة) + 1 مل من المذيب في أمبولة - عبوة من 1.
Synagis هو مجفف بالتجميد أبيض إلى أبيض مصفر.
تعليمات للطبيب
تحتوي قنينة المسحوق 50 مجم على كمية إضافية تسمح بسحب 50 مجم عند إعادة التكوين إذا اتبعت التعليمات أدناه.
لإعادة التركيب ، قم بإزالة رفرف الألومنيوم من غطاء القنينة ونظف السدادة باستخدام 70٪ من الإيثانول أو ما يعادله.
أضف ببطء 0.6 مل من الماء للحقن على طول الجدار الداخلي للقارورة لتجنب الرغوة. بعد إضافة الماء ، قم بإمالة القارورة برفق وقم بتدويرها برفق لمدة 30 ثانية.
لا تهز القارورة.
يجب أن يظل محلول palivizumab في درجة حرارة الغرفة لمدة 20 دقيقة على الأقل حتى يصبح واضحًا. لا يحتوي محلول Palivizumab على مواد حافظة ويجب تناوله في غضون 3 ساعات من التحضير. قنينة تستخدم مرة واحدة. تجاهل أي دواء غير مستخدم.
بمجرد إعادة التكوين وفقًا للتعليمات ، يكون التركيز النهائي 100 مجم / مل.
يجب عدم خلط Palivizumab مع منتجات طبية أو مواد مخففة أخرى غير الماء للحقن.
يتم إعطاء Palivizumab مرة واحدة في الشهر للاستخدام العضلي ، ويفضل أن يكون ذلك في الجانب الأمامي الوحشي للفخذ. لا ينبغي استخدام عضلة الألوية بشكل روتيني كموقع للحقن لأنها يمكن أن تلحق الضرر بالعصب الوركي. يجب أن يتم الحقن بتقنية التعقيم القياسية ، ويجب أن تعطى الكميات الطبية التي تزيد عن 1 مل في جرعات مقسمة.
عند استخدام palivizumab 100 مجم / مل ، فإن الحجم (بالملل) من palivizumab يجب إعطاؤه على فترات شهر واحد = [وزن المريض بالكيلو جرام] مضروبًا في 0.15
على سبيل المثال ، بالنسبة لطفل يبلغ وزن جسمه 3 كجم ، يصبح الحساب:
(3 × 0.15) مل = 0.45 مل باليفيزوماب شهريًا.
نشرة حزمة المصدر: AIFA (وكالة الأدوية الإيطالية). تم نشر المحتوى في يناير 2016. المعلومات الموجودة قد لا تكون محدثة.
للوصول إلى أحدث إصدار ، يُنصح بالوصول إلى موقع AIFA (وكالة الأدوية الإيطالية). إخلاء المسؤولية والمعلومات المفيدة.
01.0 اسم المنتج الطبي
SYNAGIS 50 MG مسحوق ومذيب لمحلول الحقن
02.0 التركيب النوعي والكمي
تحتوي كل قنينة على 50 ملغ من باليفيزوماب * ، توفر 100 ملغ / مل من باليفيزوماب عند إعادة التركيب على النحو الموصى به.
* Palivizumab عبارة عن جسم مضاد أحادي النسيلة مؤتلف يتم إنتاجه بواسطة تقنية الحمض النووي في الخلايا المضيفة للورم النخاعي في الفئران.
للحصول على قائمة كاملة من السواغات ، انظر القسم 6.1.
03.0 الشكل الصيدلاني
مسحوق ومذيب لمحلول الحقن.
المسحوق من أبيض إلى أبيض مصفر بالتجميد.
04.0 المعلومات السريرية
04.1 المؤشرات العلاجية
يشار إلى Synagis في الوقاية من أمراض الجهاز التنفسي السفلي الحادة التي تتطلب دخول المستشفى بسبب الفيروس المخلوي التنفسي (RSV) في الأطفال المعرضين لخطر الإصابة بمرض RSV:
• الأطفال المولودين بعمر حمل 35 أسبوعًا أو أقل وأقل من 6 أشهر في وقت ظهور الفاشية الموسمية للفيروس المخلوي التنفسي.
• الأطفال الذين تقل أعمارهم عن سنتين والذين تم علاجهم من خلل التنسج القصبي الرئوي خلال الأشهر الستة الماضية.
• الأطفال الذين تقل أعمارهم عن سنتين والذين يعانون من أمراض القلب الخلقية ذات الأهمية الديناميكية الدموية.
04.2 الجرعة وطريقة الإدارة
الجرعة
الجرعة الموصى بها من Palivizumab هي 15 ملغ لكل رطل من الجسم ، تعطى مرة واحدة في الشهر خلال الفترات التي يتوقع فيها خطر RSV في المجتمع.
حجم (بالملل) من palivizumab تدار على فترات شهر واحد = [وزن المريض بالكيلوغرام] مضروبا في 0.15.
كلما كان ذلك ممكنا ، يجب إعطاء الجرعة الأولى قبل بداية الموسم الحرج.يجب إعطاء الجرعات اللاحقة مرة واحدة في الشهر خلال فترة الخطر. لم يتم إثبات فعالية palivizumab بجرعات أخرى غير 15 ملغ لكل كيلوغرام. أو في مختلفة جرعات من مرة واحدة في الشهر خلال موسم RSV.
تم اكتساب معظم التجارب ، بما في ذلك التجارب السريرية الرئيسية في المرحلة الثالثة ، مع palivizumab من خلال 5 حقن خلال موسم واحد (انظر القسم 5.1). تتوفر البيانات ، على الرغم من محدوديتها ، عن أكثر من 5 جرعات (انظر القسمين 4.8 و 5.1) ، وبالتالي لم يتم تحديد فائدة الحماية التي تزيد عن 5 جرعات.
لتقليل مخاطر الدخول المتكرر إلى المستشفى ، في الأطفال الذين يتناولون palivizumab الذين تم إدخالهم إلى المستشفى بسبب RSV ، يوصى بمواصلة جرعات palivizumab الشهرية طوال فترة موسم الفيروس.
بالنسبة للأطفال الذين يخضعون لعملية تحويل مسار القلب ، يوصى بحقن 15 مجم / كجم من وزن الجسم من palivizumab بمجرد استقراره بعد الجراحة لضمان مستويات كافية في مصل palivizumab. يجب استئناف الجرعات اللاحقة شهريًا أثناء العلاج. المتبقي من موسم RSV للأطفال الذين لا يزالون معرضين لخطر الإصابة بفيروس RSV (انظر القسم 5.2).
طريقة الإعطاء
تدار Palivizumab عن طريق الحقن العضلي ، ويفضل أن يكون ذلك في الجانب الأمامي الوحشي للفخذ. لا ينبغي استخدام عضلة الألوية في كثير من الأحيان كموقع للحقن لأنها يمكن أن تلحق الضرر بالعصب الوركي. يجب أن يتم "الحقن" باستخدام تقنية التعقيم القياسية.
يجب أن تدار الكميات الأكبر من 1 مل في جرعات مقسمة.
للتأكد من إعادة تكوين الحجم الصحيح لـ Synagis ، راجع القسم 6.6.
04.3 موانع الاستعمال
فرط الحساسية للمادة الفعالة أو لأي من السواغات المدرجة في القسم 6.1 ، أو للأجسام المضادة وحيدة النسيلة المتوافقة مع البشر.
04.4 تحذيرات خاصة واحتياطات مناسبة للاستخدام
تم الإبلاغ عن ردود الفعل التحسسية بما في ذلك حالات نادرة جدًا من الحساسية المفرطة وصدمة الحساسية بعد إعطاء palivizumab. في بعض الحالات ، تم الإبلاغ عن حالات وفاة (انظر القسم 4.8).
يجب أن تكون الأدوية المستخدمة لعلاج تفاعلات فرط الحساسية الشديدة ، بما في ذلك الحساسية المفرطة والصدمة التأقية ، متاحة للاستخدام فورًا بعد إعطاء palivizumab.
قد يتم تأجيل استخدام palivizumab في حالة وجود عدوى شديدة أو معتدلة أو في وجود مرض حموي ، إلا إذا قرر الطبيب تأجيل إعطاء palivizumab كعامل خطر إضافي. متلازمة الحمى المعتدلة ، على سبيل المثال ، الجهاز التنفسي العلوي الخفيف العدوى ، عادة لا تؤدي إلى تأجيل إدارة palivizumab.
يجب إعطاء Palivizumab بحذر في المرضى الذين يعانون من قلة الصفيحات أو مشاكل التخثر الأخرى.
لم يتم تقييم فعالية palivizumab عند إعطائه للمرضى كدورة ثانية للوقاية خلال موسم وباء RSV جديد في دراسة بهذا الهدف. مع palivizumab لم يتم استبعاده نهائيًا مع دراسات لتقييم هذا الجانب بالذات.
04.5 التفاعلات مع المنتجات الطبية الأخرى وأشكال التفاعل الأخرى
لم يتم إجراء دراسات تفاعل محددة مع المنتجات الطبية الأخرى. في التجارب السريرية للمرحلة الثالثة على حدوث RSV في الأطفال المولودين قبل الأوان ومع خلل التنسج القصبي الرئوي ، أظهر المرضى الذين يتلقون العلاج الوهمي والمرضى الذين تلقوا لقاحات الطفولة الروتينية ولقاح الأنفلونزا وموسعات الشعب الهوائية أو الكورتيكوستيرويدات توزيعًا مشابهًا ولم تظهر أي زيادات في لوحظت ردود فعل سلبية.
نظرًا لأن الجسم المضاد وحيد النسيلة خاص بالفيروس المخلوي التنفسي ، فمن غير المتوقع أن يتداخل palivizumab مع الاستجابة المناعية للقاحات.
قد يتداخل Palivizumab مع اختبارات تشخيص RSV القائمة على المناعة ، مثل بعض الاختبارات المستندة إلى المستضد. بالإضافة إلى ذلك ، يمنع palivizumab تكاثر الفيروس في ثقافة الخلية وبالتالي قد يتداخل أيضًا مع اختبارات الثقافة الفيروسية. لا يتداخل Palivizumab مع اختبارات تفاعل البوليميراز المتسلسل للنسخ العكسي. قد يؤدي التداخل مع الاختبارات إلى نتائج اختبار تشخيص RSV سلبية كاذبة ، لذلك يجب استخدام نتائج الاختبارات التشخيصية ، عند الحصول عليها ، مع النتائج السريرية لتوجيه القرارات الطبية.
04.6 الحمل والرضاعة
غير ذات صلة. Synagis غير محدد للاستخدام في البالغين ، ولا توجد بيانات عن الخصوبة ، واستخدامها في الحمل والرضاعة.
04.7 التأثيرات على القدرة على السياقة واستعمال الآلات
غير ذات صلة.
04.8 الآثار غير المرغوب فيها
ملخص ملف تعريف السلامة
أخطر ردود الفعل السلبية التي تحدث مع palivizumab هي الحساسية المفرطة وغيرها من تفاعلات فرط الحساسية الحادة. التفاعلات الجانبية الأكثر شيوعًا التي تحدث مع palivizumab هي الحمى والطفح الجلدي ورد فعل موقع الحقن.
جدول التفاعلات العكسية
يتم سرد التفاعلات العكسية السريرية والمخبرية ، التي حدثت في الدراسات التي أجريت على المرضى المبتسرين والأطفال المصابين بخلل التنسج القصبي الرئوي وفي المرضى الذين يعانون من أمراض القلب الخلقية لدى الأطفال ، حسب فئة أعضاء النظام وتواترها (شائع جدًا 1/10 ؛ شائع 1/100 في
يتم الإبلاغ عن ردود الفعل السلبية التي تم تحديدها من خلال مراقبة ما بعد التسويق طواعية من مجموعة ذات حجم غير مؤكد ؛ ليس من الممكن دائمًا تقدير تواترها بشكل موثوق أو إنشاء علاقة سببية مع تعرض palivizumab. تم تقدير تواتر هذه التفاعلات الضائرة (ARs) ، كما هو مذكور في الجدول أدناه ، باستخدام بيانات السلامة من الدراستين السريريتين. أظهرت التفاعلات في هذه الدراسات عدم وجود فرق بين مجموعتي palivizumab والعلاج الوهمي ولم تكن التفاعلات مرتبطة بالدواء.
* للحصول على وصف كامل للدراسة ، انظر القسم 5.1 الدراسات السريرية
# RAs التي تم تحديدها من خلال مراقبة ما بعد التسويق
وصف ردود الفعل السلبية المختارة
تجربة ما بعد التسويق
تم تقييم ردود الفعل السلبية العفوية الخطيرة بعد التسويق التي تم الإبلاغ عنها أثناء علاج palivizumab بين عامي 1998 و 2002 والتي تغطي أربعة مواسم وبائية RSV. تم تلقي ما مجموعه 1291 تقريرًا خطيرًا حيث تم إعطاء palivizumab كما هو محدد وكانت مدة العلاج أكثر من موسم واحد.حدثت ردود الفعل السلبية بعد الجرعة السادسة أو أكثر ، في 22 من هذه التقارير فقط. (15 بعد الجرعة السادسة ، 6 بعد الجرعة السابعة و 1 بعد الجرعة الثامنة). هذه التفاعلات الضائرة لها خصائص مشابهة لتلك التي تحدث بعد الجرعات الخمس الأولية.
تم رصد الجدول الزمني للعلاج باليفيزوماب وردود الفعل السلبية في مجموعة تضم ما يقرب من 20000 طفل تم اتباعها من خلال برنامج التزام المريض بين عامي 1998 و 2000. ومن بين هذه المجموعة ، تلقى 1250 طفلًا مسجلاً 6 حقن. 183 كان لديهم 7 و 27 لديهم 8 أو 9. ردود الفعل السلبية لوحظ في المرضى بعد الجرعة السادسة أو أكثر لها خصائص وتكرار مماثل لتلك التي بعد الجرعات الخمس الأولية.
في دراسة ما بعد التسويق القائمة على الملاحظة القائمة على قاعدة البيانات ، لوحظت زيادة طفيفة في تواتر الربو بين المرضى الخدج الذين عولجوا باستخدام palivizumab ؛ ومع ذلك ، فإن العلاقة السببية غير مؤكدة.
الإبلاغ عن ردود الفعل السلبية المشتبه بها
يعد الإبلاغ عن ردود الفعل السلبية المشتبه بها التي تحدث بعد الترخيص للمنتج الطبي أمرًا مهمًا لأنه يسمح بالمراقبة المستمرة لنسبة الفائدة / المخاطر للمنتج الطبي. يُطلب من المتخصصين في الرعاية الصحية الإبلاغ عن أي ردود فعل سلبية مشتبه بها عبر موقع وكالة الأدوية الإيطالية. : www.agenziafarmaco.gov.it/it/responsabili.
04.9 جرعة زائدة
في التجارب السريرية ، تم إعطاء ثلاثة أطفال جرعات أعلى من 15 مجم / كجم. كانت هذه الجرعات 20.25 مجم / كجم و 21.1 مجم / كجم و 22.27 مجم / كجم. لم تكن هناك عواقب سريرية في هذه المواضيع.
من تجربة ما بعد التسويق ، تم الإبلاغ عن جرعات زائدة بجرعات تصل إلى 85 مجم / كجم وفي بعض الحالات ، لم تكن التفاعلات الضائرة المبلغ عنها مختلفة عن تلك التي لوحظت مع جرعة 15 مجم / كجم (انظر القسم 4.8). يوصى بمراقبة المريض بحثًا عن أي علامات أو أعراض لردود فعل سلبية أو آثار وبدء العلاج المناسب للأعراض على الفور.
05.0 الخصائص الصيدلانية
05.1 الخصائص الديناميكية الدوائية
مجموعة العلاج الدوائي: الغلوبولين المناعي في الدم ، الغلوبولين المناعي المحدد.
كود ATC J06BB16.
Palivizumab هو جسم مضاد أحادي النسيلة IgG1K موجه ضد حاتمة في موقع المستضد A لبروتين اندماج الفيروس التنفسي المخلوي (RSV). يحتوي هذا الجسم المضاد الوحيد النسيلة المتوافق مع البشر على تسلسل جسم مضاد بشري (95٪) وفأري (5٪). له نشاط معادل وتثبيط قوي لآليات الاندماج ضد VRS في كل من النوع الفرعي A والسلالات الفرعية B.
في فئران القطن ، تبين أن تركيزات palivizumab في الدم التي تبلغ حوالي 30 ميكروغرام / مل تنتج انخفاضًا بنسبة 99 ٪ في تكرار RSV في الرئتين.
تعليم في المختبر من النشاط المضاد للفيروسات
تم تقييم النشاط المضاد للفيروسات لـ palivizumab في اختبار تحييد دقيق حيث تم تحضين تركيزات الأجسام المضادة المتزايدة باستخدام RSV قبل إضافة الخلايا الظهارية HEp-2 البشرية. بعد فترة حضانة مدتها 4-5 أيام ، تم قياس مستضد VRS في مقايسة مناعية إنزيمية (ELISA). يتم التعبير عن عيار التعادل (تركيز فعال بنسبة 50٪ [EC50]) على أنه تركيز الجسم المضاد القادر على تقليل اكتشاف مستضد VRS بواسطة 50٪ مقارنة بالخلايا المصابة بالفيروس غير المعالجة. يُظهر Palivizumab متوسط قيم EC50 بقيمة 0.65 ميكروغرام / مل (يعني [الانحراف المعياري] = 0.75 [0.53] ميكروغرام / مل ، n = 69 ، النطاق 0.07-2.89 ميكروغرام / مل) و 0.28 ميكروغرام / مل (يعني [الانحراف المعياري] ] = 0.35 [0.23] ميكروغرام / مل ، ن = 35 ، المدى 0.03-0.88 ميكروغرام / مل) ، في RSV A و RSV B ، على التوالي العزلات السريرية. تم جمع معظم العزلات السريرية RSV المختبرة (ن = 96) من أفراد في الولايات المتحدة.
المقاومة
يرتبط Palivizumab بمنطقة محمية للغاية في المجال خارج الخلية لبروتين RSV الناضج F ، والمشار إليه بالموقع المستضدي II أو موقع المستضد A ، والذي يتضمن الأحماض الأمينية 262-275. تحليل النمط الجيني الذي تم إجراؤه على 126 عزلة إكلينيكية من 123 طفلاً فشلوا في الوقاية المناعية ، أظهرت جميع طفرات RSV التي تظهر مقاومة ضد palivizumab (n = 8) تغيرات في الأحماض الأمينية في هذه المنطقة من البروتين F. تسلسل خارج موقع المستضد A لبروتين VRS F الذي يجعل RSV مقاومًا للتحييد بواسطة palivizumab. تم تحديد مقاومة palivizumab واحدة على الأقل مرتبطة ببدائل الأحماض الأمينية N262D أو K272E / Q أو S275F / L في هذه العزلات السريرية الثماني RSV مما أدى إلى تردد مقاومة مرتبط بالطفرة بنسبة 6.3 ٪. أظهر تحليل البيانات السريرية عدم وجود "ارتباط بين التغيرات في تسلسل الموقع المستضدي A وشدة مرض RSV في الأطفال الذين يتلقون الوقاية المناعية Palivizumab وتطور مرض الجهاز التنفسي السفلي RSV." وجدت 254 عزلة إكلينيكية RSV تم جمعها من الأشخاص الساذجين للوقاية المناعية مقاومة لـ palivizumab المرتبطة ببدائلين. (1 مع N262D و 1 مع S275F) ، مما ينتج عنه تردد مقاومة مرتبط بالطفرة بنسبة 0.79٪.
المناعة
تم العثور على الأجسام المضادة لـ palivizumab في حوالي 1 ٪ من المرضى في دراسة Impact-RSV خلال المرحلة الأولى من العلاج.كانت ظاهرة عابرة ذات عيار منخفض ، تم حلها على الرغم من استمرار الاستخدام (الموسمين الأول والثاني) ، ولم يتم تسليط الضوء عليها. على 55 من 56 رضيعًا خلال الموسم الثاني (بما في ذلك 2 مع المعايرة خلال الموسم الأول).
لم يتم التحقيق في الاستمناع في دراسة أمراض القلب الخلقية.
تم تقييم الأجسام المضادة لـ palivizumab في أربع دراسات إضافية في 4337 مريضًا (الرضع المولودين في 35 أسبوعًا من الحمل أو أقل و 6 أشهر من العمر أو أقل ، أو 24 شهرًا أو أقل مع خلل التنسج القصبي الرئوي ، أو يعانون من أمراض القلب الخلقية الديناميكية الدموية الهامة. عند تضمينها في هذه الدراسات) ولوحظت في 0٪ - 1.5٪ من المرضى في فترات الدراسة المختلفة. لم يلاحظ أي ارتباط بين وجود الأجسام المضادة والأحداث السلبية.
لذلك ، فإن الاستجابات المناعية للأجسام المضادة للأدوية (مضاد للأجسام المضادة للمخدرات، ADA) غير ذات صلة سريريًا.
الدراسات السريرية مع palivizumab المجففة بالتجميد
في دراسة سريرية خاضعة للتحكم الوهمي في الوقاية من RSV (دراسة تأثير RSV) أجريت على 1502 من الأطفال المعرضين لمخاطر عالية (1002 Synagis ، 500 دواء وهمي) ، خفضت 5 جرعات شهرية من 15 مجم / كجم من حدوث الاستشفاء المتعلق بـ VRS بنسبة 55 ٪ (ع =
كان معدل الاستشفاء بسبب الفيروس المخلوي التنفسي في مجموعة الدواء الوهمي 10.6 ٪. على هذا الأساس ، فإن الحد من المخاطر المطلقة هو 5.8 ٪ مما يعني أن عدد المرضى الذين يجب علاجهم لمنع الاستشفاء هو 17. شدة الإصابة بفيروس RSV في الأطفال في المستشفى ، على الرغم من العلاج الوقائي palivizumab ، لا من حيث النسبة المئوية ولا أيام العلاج في المستشفى في العناية المركزة ولا أيام التنفس الميكانيكي المساعد.
تم تسجيل ما مجموعه 222 طفلاً في دراستين منفصلتين لفحص سلامة palivizumab عند إعطائه للموسم الثاني RSV. تلقى مائة وثلاثة أطفال حقن باليفيزوماب شهريًا لأول مرة ، وتلقى 119 طفلاً دواء باليفيزوماب لموسمين متتاليين. لم يكن هناك فرق بين المجموعات في الاستمناع في أي من الدراستين.ومع ذلك ، حيث لم يتم التحقيق رسميًا في فعالية palivizumab عند إعطائه للمرضى كدورة علاجية ثانية خلال بداية موسم RSV. من هذه البيانات من حيث الفعالية غير معروف.
في دراسة سريرية مستقبلية مفتوحة التسمية مصممة لتقييم الحرائك الدوائية والسلامة والمناعة بعد إعطاء 7 جرعات من palivizumab خلال موسم RSV واحد ، أشارت بيانات الحرائك الدوائية إلى أنه تم الوصول إلى مستويات كافية من palivizumab في جميع الأطفال الذين تم تجنيدهم وعددهم 18. لوحظت مستويات منخفضة وعابرة من الأجسام المضادة للأجسام المضادة لـ palivizumab في الطفل بعد الجرعة الثانية من palivizumab وانخفضت هذه الأجسام المضادة إلى مستوى غير قابل للقياس عند الجرعة الخامسة والسابعة.
في دراسة خاضعة للتحكم الوهمي على 1287 مريضًا بعمر 24 شهرًا يعانون من أمراض القلب الخلقية ذات الأهمية الديناميكية الدموية (639 Synagis ؛ 648 دواء وهمي) ، قللت 5 جرعات شهرية من 15 مجم / كجم من Synagis من حدوث الاستشفاء RSV بنسبة 45 ٪ (P = 0.003 ) (دراسة أمراض القلب الخلقية) كانت المجموعات متوازنة بالتساوي بين مرضى الزرقة وغير المزرقة. كان معدل الاستشفاء RSV 9.7٪ في مجموعة الدواء الوهمي و 5.3٪ في مجموعة Synagis. وأظهر الهدف الثاني من دراسة الفعالية على 100 طفل انخفاض كبير في مجموعة Synagis مقارنة بمجموعة الدواء الوهمي في إجمالي أيام الاستشفاء من أجل RSV (انخفاض بنسبة 56٪ ، p = 0.003) وعلى العدد الإجمالي لأيام RSV مع l "إضافة مكمل أكسجين (انخفاض بنسبة 73٪ ، ص = 0.014).
تم إجراء دراسة قائمة على الملاحظة بأثر رجعي على الأطفال الذين يعانون من أمراض القلب الخلقية الهامة ديناميكيًا (HSCHD) لمقارنة حدوث الأحداث الضائرة الأولية الخطيرة (العدوى ، وعدم انتظام ضربات القلب ، والوفاة) بين أولئك الذين تلقوا العلاج الوقائي Synagis وأولئك الذين لم يتلقوه معًا بسبب العمر ، نوع إصابة القلب والجراحة التصحيحية السابقة. كانت حالات عدم انتظام ضربات القلب والوفاة متشابهة في كل من الأطفال الذين تلقوا العلاج الوقائي والأطفال الذين لم يفعلوا ذلك. "كانت نسبة الإصابة بالعدوى أقل في الأطفال الذين تلقوا العلاج الوقائي مقارنة بأولئك الذين لم يفعلوا ذلك." تشير النتائج إلى أن خطر الإصابة بالعدوى الشديدة ، أو عدم انتظام ضربات القلب الحاد أو الوفاة لدى الأطفال المصابين بأمراض القلب الخلقية الهامة ديناميكيًا المرتبطة بالوقاية من Synagis لم تزداد مقارنة بالأطفال الذين لم يتلقوا الملف الشخصي المحاور.
دراسات باستخدام السائل palivizumab
تم إجراء دراستين سريريتين للمقارنة المباشرة بين التركيبات السائلة والمجففة بالتجميد من palivizumab. في الدراسة الأولى ، تلقى جميع الأطفال الخدج البالغ عددهم 153 خديجًا كلا الصيغتين بتسلسلات مختلفة. في الدراسة الثانية ، تلقى 211 و 202 من الأطفال الخدج أو الأطفال المصابين بأمراض الرئة المزمنة سائلًا ومجفف بالتجميد باليفيزوماب ، على التوالي. في دراستين إضافيتين ، تم استخدام palivizumab السائل كعنصر تحكم نشط (3918 موضوعًا للأطفال) لتقييم الأجسام المضادة أحادية النسيلة التجريبية للوقاية من مرض RSV الشديد عند الرضع الخدج أو الأطفال المصابين بأمراض الرئة المزمنة أو أمراض القلب. مهم ديناميكيًا (انظر أدناه لمزيد من التفاصيل في هاتين الدراستين). كان المعدل العام ونمط الأحداث الضائرة ، وتحليل التوقف عن العلاج بسبب الأحداث الضائرة ، وعدد الوفيات المبلغ عنها في هذه الدراسات السريرية متسقة مع تلك التي لوحظت خلال برامج التطوير السريري للتركيبة المجففة بالتجميد. ولم يتم تحديد أي أحداث سلبية جديدة في هذه الدراسات.
الخدج والأطفال المصابون بمرض الرئة الخداج المزمن (BPD): أجريت هذه الدراسة في 347 مركزًا في أمريكا الشمالية والاتحاد الأوروبي و 10 دول أخرى ، ودرس المرضى الذين تتراوح أعمارهم بين 24 شهرًا أو أقل المصابين باضطراب الشخصية الحدية والمرضى الذين يعانون من ولادة مبكرة (أقل من أو يساوي 35 أسبوعًا من الحمل) ، الذين كانوا 6 أشهر أو أقل عند بدء الدراسة. تم استبعاد المرضى الذين يعانون من أمراض القلب الخلقية ذات الأهمية الديناميكية الدموية من هذه الدراسة وتم فحصهم في دراسة منفصلة في هذه الدراسة ، تم اختيار المرضى عشوائياً لتلقي 5 شهريًا حقن 15 ملجم / كجم من سائل باليفيزوماب (N = 3306) ، يستخدم كعنصر تحكم فعال لجسم مضاد أحادي النسيلة (N = 3329) ، تمت مراقبة السلامة والفعالية في هذه الموضوعات لمدة 150 يومًا. أكمل ثمانية وتسعون في المائة من جميع المرضى الذين تلقوا palivizumab الدراسة ، وتلقى 97 ٪ جميع الحقن الخمس. كانت نقطة النهاية الأولية هي حدوث الاستشفاء من RSV. حدثت حالات دخول المستشفى RSV بين 62 من 3306 (1.9 ٪) من المرضى في مجموعة palivizumab. كان معدل الاستشفاء المرصود لـ RSV في المرضى المسجلين بتشخيص BPD 28 من 723 (3.9 ٪) وفي المرضى المسجلين بتشخيص الخداج دون BPD كان 34 من 2583 (1.3 ٪).
دراسة 2 CHD: هذه الدراسة ، التي أجريت في 162 مركزًا في أمريكا الشمالية والاتحاد الأوروبي و 4 دول أخرى ، لأكثر من موسمين من RSV ، درست المرضى الذين يبلغ عمرهم 24 شهرًا أو أقل والذين يعانون من أمراض الشرايين التاجية المهمة ديناميكيًا. لتلقي 5 حقن شهرية من 15 مجم / كجم من سائل palivizumab (N = 612) ، يستخدم كعنصر تحكم نشط في جسم مضاد أحادي النسيلة (N = 624). تم تقسيم الموضوعات إلى طبقات بناءً على إصابة القلب (الزرقة مقابل غيرها) والسلامة وتم رصد الفعالية لمدة 150 يومًا. أكمل سبعة وتسعون بالمائة من جميع المرضى الذين تلقوا palivizumab الدراسة ، وتلقى 95 بالمائة جميع الحقن الخمس. كانت نقطة النهاية الأولية عبارة عن ملخص للأحداث الضائرة والأحداث الضائرة الخطيرة ، وكانت نقطة النهاية الثانوية هي حدوث دخول المستشفى RSV. كان معدل حدوث الاستشفاء RSV 16 من 612 (2.6 ٪) في مجموعة palivizumab.
05.2 خصائص حركية الدواء
صياغة باليفيزوماب المجففة بالتبريد
في الدراسات التي أجريت على متطوعين بالغين ، أظهر palivizumab مظهرًا حركيًا دوائيًا مشابهًا للجسم المضاد IgG1 البشري فيما يتعلق بحجم التوزيع (متوسط 57 مل / كجم) ونصف العمر (متوسط 18 يومًا).في دراسات الوقاية في الأطفال الخدج المصابين بخلل التنسج القصبي الرئوي ، كان متوسط عمر النصف لـ palivizumab 20 يومًا والجرعات الشهرية في العضل البالغة 15 مجم / كجم حققت تركيزات مصلية من المادة الفعالة في اليوم 30 تبلغ حوالي 40 ميكروغرام / مل. بعد الحقن الأول ، حوالي 60 ميكروغرام / مل بعد الحقن الثاني ، حوالي 70 ميكروغرام / مل بعد الحقن الثالث والرابع.في دراسة أمراض القلب الخلقية ، بلغت الجرعات الشهرية في العضل 15 ملغ / كغ بمتوسط 30 يوماً كحد أدنى. قيمة تركيزات المصل الفعال للمكون الفعال 55 ميكروغرام / مل بعد الحقن الأول وحوالي 90 ميكروغرام / مل بعد الحقن الرابع.
في دراسة أمراض القلب الخلقية ، من بين ما يقرب من 139 طفلًا تلقوا palivizumab ، في أولئك الذين خضعوا لمجرى قلبية رئوية والذين توفرت لهم عينات مصل مزدوجة ، كان متوسط تركيز مصل palivizumab حوالي 100 ميكروغرام / مل قبل المجازة القلبية وانخفض إلى ما يقرب من 40 ميكروغرام / مل بعد الالتفافية.
05.3 بيانات السلامة قبل السريرية
في دراسات السموم أحادية الجرعة التي أجريت على القرود (الجرعة القصوى 30 مجم / كجم) والأرانب (الجرعة القصوى 50 مجم / كجم) والجرذان (الجرعة القصوى 840 مجم / كجم) ، لم يتم العثور على بيانات مهمة.
الدراسات التي أجريت على القوارض لم تظهر زيادة في تكاثر RSV ، أو الأمراض التي يسببها RSV أو توليد فيروسات متحولة في وجود palivizumab في ظل الظروف التجريبية المعتمدة.
06.0 المعلومات الصيدلانية
06.1 السواغات
تراب:
الهيستيدين
جليكاين
مانيتول (E421)
مذيب:
ماء للحقن.
06.2 عدم التوافق
يجب عدم خلط هذا المنتج الطبي مع منتجات طبية أو مواد مخففة أخرى غير الماء للحقن.
06.3 فترة الصلاحية
4 سنوات.
بعد إعادة التركيب ، يجب استخدام المنتج الطبي على الفور. في أي حال ، تم إثبات الثبات في ظل ظروف الاستخدام لمدة 3 ساعات عند 20-24 درجة مئوية.
06.4 احتياطات خاصة للتخزين
يحفظ في الثلاجة (2 درجة مئوية - 8 درجة مئوية).
لا تجمد.
احفظ القارورة في الكرتون الخارجي لحمايتها من الضوء.
06.5 طبيعة العبوة الفورية ومحتويات العبوة
50 ملغ من المسحوق في قنينة 4 مل (زجاج من النوع الأول) مع سدادة (مطاط بوتيل) وختم (ألومنيوم).
1 مل من الماء للحقن في قنينة (زجاج من النوع الأول).
عبوة من قطعة واحدة.
06.6 تعليمات الاستخدام والتداول
تحتوي قنينة المسحوق 50 مجم على كمية إضافية تسمح بسحب 50 مجم عند إعادة التكوين إذا اتبعت التعليمات أدناه.
لإعادة التركيب ، قم بإزالة رفرف الألومنيوم من غطاء القنينة ونظف السدادة باستخدام 70٪ من الإيثانول أو ما يعادله.
أضف ببطء 0.6 مل من الماء للحقن على طول الجدار الداخلي للقارورة لتجنب الرغوة. بعد إضافة الماء ، قم بإمالة القارورة قليلاً وحركها برفق لمدة 30 ثانية. لا تهز القارورة. يجب أن يظل محلول palivizumab في درجة حرارة الغرفة لمدة 20 دقيقة على الأقل حتى يصبح واضحًا. لا يحتوي محلول Palivizumab على مواد حافظة ويجب تناوله في غضون 3 ساعات من التحضير.
بمجرد إعادة التكوين وفقًا للتعليمات ، يكون التركيز النهائي 100 مجم / مل.
مظهر المحلول المعاد تكوينه واضح إلى براق قليلاً.
قنينة تستخدم مرة واحدة. يجب التخلص من الأدوية غير المستخدمة والنفايات الناتجة عن هذا الدواء وفقًا للوائح المحلية.
07.0 حامل ترخيص التسويق
أبفي المحدودة
بكارة
SL6 4XE
المملكة المتحدة
08.0 رقم ترخيص التسويق
EU / 1/99/117/001
AIC 034529014 / هـ
09.0 تاريخ أول تفويض أو تجديد التفويض
تاريخ أول ترخيص: 13 أغسطس 1999
10.0 تاريخ مراجعة النص
04/2015