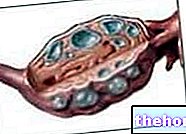
تقنية العقدة الليمفاوية الحارسة والإزالة الجراحية للغدد الليمفاوية الإبطية
أثناء الجراحة ، يتم دائمًا حقن متتبع مشع حول كتلة الورم لتحديد "العقدة الليمفاوية الحارسة" (LS) ، وهي أول عقدة ليمفاوية تجمع اللمف (أي النفايات) من موقع الورم. ، بمجرد توطينها ، لأنها البقع ذات الصبغة المشعة ، سيتم إزالتها وتحليلها تحت المجهر لمعرفة ما إذا كانت هناك خلايا سرطانية بالداخل.
إن تقييم العقدة الليمفاوية الحارسة قادر على التنبؤ بدقة بحالة العقد الليمفاوية الإقليمية الأخرى للإبط والتي ، من الناحية التشريحية ، تأتي جميعها بعد ذلك.ويترتب على ذلك أنه إذا كانت العقدة الليمفاوية الحارسة خالية من الخلايا السرطانية ، فمن الممكن تجنب إزالة العقد الليمفاوية الأخرى ، مع الاحتفاظ بهذه العملية ، وليس بدون آثار جانبية مثل تورم الذراع المستمر (الوذمة الليمفاوية) ، فقط للمرضى الذين يتأثرون حقًا بتورط الغدد الليمفاوية في النقائل (30-40٪ من الحالات).
بجانب الجراحة التي تركز على الثدي ، هناك أيضًا إزالة الغدد الليمفاوية الإبطية ، وهو أمر مفيد ليس فقط للشفاء ، ولكن أيضًا للتحكم في انتشار المرض. في الواقع ، يمثل غزو الغدد الليمفاوية الإبطية العامل التنبئي لشفاء أو عدم علاج سرطان الثدي.لذا ، فإن إزالة هذه الغدد الليمفاوية تلعب دورًا أساسيًا ويجب أن تكون جذرية في معظم مرضى السرطان الغازي. السرطانات الغازية التي يكون احتمال غزوها ضئيلًا ، كما هو الحال في الأشكال الموضعية أو الغازية حيث تم اكتشاف أن العقدة الليمفاوية الحارسة منتشرة. وقد اقترح مؤخرًا التخلي عن إزالة العقد الليمفاوية الإبطية حتى في الأشكال الورمية أصغر من سنتيمتر واحد وأورام خبيثة منخفضة.
من الضروري في الواقع اعتبار أن استئصال العقد الليمفاوية يحرم المريض من أداة دفاعية مهمة ، طورها الجسم على وجه التحديد لتكون بمثابة حاجز أمام انتشار مرض الورم.
العلاج الإشعاعي
فقط في 40٪ من الحالات يقتصر الورم على العقدة الأولية ، بينما في 60٪ توجد بؤر للورم ، في الموقع أو غازية ، وأيضًا في مواقع أخرى قريبة من الثدي. تزداد احتمالية العثور على هذه الآفات بالقرب من الورم الأساسي وتتناقص تدريجياً مع زيادة المسافة منه. يشكل هذا الأساس لتنفيذ العلاج الإشعاعي بعد التدخلات المحافظة في جميع المرضى المصابين بالسرطان الغازي ، والذي يعد جزءًا لا يتجزأ من العلاج ، وتتمثل الاستثناءات المحتملة لهذه القاعدة في المرضى المسنين المصابين بأورام صغيرة القطر وغير عدوانية وغياب. المزيد من بؤر خلايا سرطان الثدي في حالات أخرى ، إذا كانت هناك موانع أو عدم القدرة على أداء العلاج الإشعاعي ، يجب أن يكون استئصال الثدي الكلي هو العلاج الأول.
يُشار إلى العلاج الإشعاعي بعد استئصال الثدي الجذري بدلاً من ذلك في المرضى المعرضين لخطر الانتكاس العالي ، مثل أولئك الذين يعانون من إصابة عدد من الغدد الليمفاوية الإبطية أكبر من 4 ، أو مع آفات الورم واسعة النطاق.
العلاج الكيميائي
بشكل عام ، فإن الانخفاض في خطر الانتكاس والوفاة المرتبط باستخدام العلاج الكيميائي هو 23.8٪ و 15.2٪ على التوالي ، وهو أكبر بالنسبة للنساء اللائي لم يصلن بعد إلى سن اليأس مقارنة بالنساء اللاتي في سن اليأس بالفعل ، في حين أنه مستقل عما إذا كان الورم يؤثر الغدد الليمفاوية أم لا.
العلاج بالهرمونات
لمزيد من المعلومات: أدوية سرطان الثدي
تتكون بعض أنواع سرطان الثدي من خلايا حساسة للإستروجين. في ظل وجود هذه الأورام ، وبعد 5 سنوات من العلاج ، لوحظ أن الحد من خطر الانتكاس والوفيات هو على التوالي 47٪ و 26٪.
حاليا ، تدار تاموكسيفين لمدة 5 سنوات ، حيث لا يبدو أن إطالة العلاج توفر فائدة إضافية. كما يبدو أنه يقلل من الإصابة بسرطان الثدي المقابل ويمنع هشاشة العظام وأمراض القلب والأوعية الدموية. تتمثل الآثار الضارة لهذا العلاج في زيادة خطر الإصابة بسرطان بطانة الرحم والانصمام الخثاري.
متابعة
الفحص السريري والتصوير الشعاعي للثدي الدوري هما الاختباران الوحيدان اللذان يجب وصفهما لمتابعة مرضى سرطان الثدي.
المزيد من المقالات حول "سرطان الثدي: العلاج الإشعاعي والعلاج الكيميائي والعلاج الهرموني"
- سرطان الثدي: الأعراض والعلاج الجراحي
- سرطان الثدي
- سرطان الأقنية الموضعي - سرطان مفصص موضعي
- عوامل الخطر لسرطان الثدي
- سرطان الثدي والحمل
- سرطان الثدي - أدوية سرطان الثدي