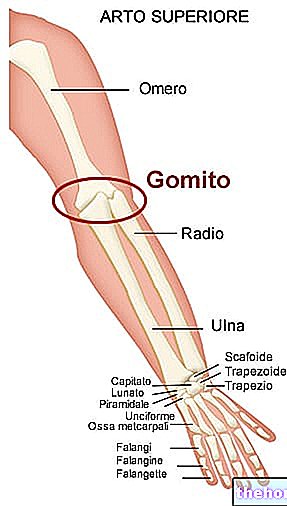
الهيكل والوظائف
الهيموجلوبين هو بروتين معدني موجود في خلايا الدم الحمراء ، وهو مسؤول عن نقل الأكسجين في مجرى الدم ، في الواقع ، الأكسجين قابل للذوبان بشكل معتدل في الماء فقط. لذلك ، فإن الكميات الذائبة في الدم (أقل من 2٪ من الإجمالي) لا تكفي لتلبية متطلبات التمثيل الغذائي للأنسجة. ولذلك فإن الحاجة إلى ناقل معين واضحة.
في مجرى الدم ، لا يمكن للأكسجين الارتباط بالبروتينات بشكل مباشر وقابل للعكس ، كما يحدث بدلاً من ذلك بالنسبة للمعادن مثل النحاس والحديد. وليس من المستغرب أن نجد ما يسمى بالبروتينات في وسط كل وحدة فرعية من البروتين للهيموجلوبين ، ملفوفة في غلاف بروتيني ، مجموعة EME ، بقلب معدني يتم تمثيله بواسطة ذرة حديد في حالة أكسدة Fe2 + (حالة مخفضة) ، والتي تربط الأكسجين بطريقة قابلة للعكس.
تحليل الدم
- قيم الهيموجلوبين الطبيعية في الدم: 13-17 جم / 100 مل
في النساء ، تكون القيم أقل بنسبة 5-10٪ في المتوسط من الرجال.
الأسباب المحتملة لارتفاع نسبة الهيموجلوبين
- كثرة الحمر
- إقامة ممتدة على أرض مرتفعة
- أمراض الرئة المزمنة
- مرض قلبي
- المنشطات الدموية (استخدام الإريثروبويتين ومشتقاته أو المواد التي تحاكي عملهم)
الأسباب المحتملة لانخفاض نسبة الهيموجلوبين
- فقر الدم
- نقص الحديد (نقص الحديد)
- نزيف غزير
- السرطانات
- حمل
- التلاسيمية
- الحروق
لذلك يتم إعطاء محتوى الأكسجين في الدم من خلال تجميع الكمية الصغيرة الذائبة في البلازما مع الجزء المرتبط بحديد الهيموجلوبين.
يرتبط أكثر من 98٪ من الأكسجين الموجود في الدم بالهيموجلوبين ، والذي يدور بدوره في مجرى الدم المخصص داخل خلايا الدم الحمراء ، لذلك بدون الهيموجلوبين ، لا تستطيع كريات الدم الحمراء أداء مهمتها كناقل للأكسجين في الدم.
بالنظر إلى الدور المركزي لهذا المعدن ، يتطلب تخليق الهيموجلوبين كمية كافية من الحديد في النظام الغذائي. حوالي 70٪ من الحديد الموجود في الجسم موجود في مجموعات الهيموغلوبين.
يتكون الهيموغلوبين من 4 وحدات فرعية تشبه هيكليًا إلى حد كبير الميوجلوبين *.
* بينما ينقل الهيموغلوبين الأكسجين من الرئتين إلى الأنسجة ، يحمل الميوغلوبين الأكسجين الذي يطلقه الهيموغلوبين إلى العضيات الخلوية المختلفة التي تستخدمه (مثل الميتوكوندريا).

الهيموغلوبين هو بروتين معدني كبير ومعقد ، يتميز بأربع سلاسل بروتين كروية ملفوفة على التوالي حول مجموعة الهيم التي تحتوي على Fe2 +.
لذلك نجد لكل جزيء هيموجلوبين أربع مجموعات هيم ملفوفة في سلسلة البروتينات الكروية النسبية. نظرًا لوجود أربع ذرات حديد في كل جزيء هيموجلوبين ، يمكن لكل جزيء هيموجلوبين ربط أربع ذرات أكسجين بنفسه ، وفقًا للتفاعل القابل للعكس:
Hb + 4O2 → → Hb (O2) 4
كما هو معروف لمعظم الناس ، فإن مهمة الهيموجلوبين هي أخذ الأكسجين في الرئتين ، وإطلاقه إلى الخلايا التي تحتاجه ، وأخذ ثاني أكسيد الكربون منها وإطلاقه في الرئتين حيث يبدأ تشيلو مرة أخرى.
أثناء مرور الدم في الشعيرات الدموية للحويصلات الهوائية الرئوية ، يربط الهيموغلوبين الأكسجين بنفسه ، والذي يطلق لاحقًا إلى الأنسجة في الدورة الدموية الطرفية. يحدث هذا التبادل لأن روابط الأكسجين مع الحديد من مجموعة EME متقاربة وحساسة للعديد من العوامل ، وأهمها التوتر أو الضغط الجزئي للأكسجين.
ارتباط الأكسجين بالهيموجلوبين وتأثير بوهر
في الرئتين ، يزداد توتر الأكسجين في البلازما بسبب انتشار الغاز من الحويصلات الهوائية إلى الدم (↑ PO2) ؛ تؤدي هذه الزيادة إلى ارتباط الهيموجلوبين بالأكسجين بشدة ؛ يحدث العكس في الأنسجة المحيطية ، حيث ينخفض تركيز الأكسجين المذاب في الدم (↓ PO2) ويزداد الضغط الجزئي لثاني أكسيد الكربون (↑ CO2) ؛ هذا يحث الهيموجلوبين على إطلاق الأكسجين ويصبح مشحونًا بثاني أكسيد الكربون. تبسيط المفهوم قدر الإمكان ، كلما زاد وجود ثاني أكسيد الكربون في الدم ، قل الأكسجين الذي يظل مرتبطًا بالهيموجلوبين.
على الرغم من أن كمية الأكسجين المذابة جسديًا في الدم منخفضة جدًا ، إلا أنها تلعب دورًا أساسيًا. في الواقع ، تؤثر هذه الكمية بشكل كبير على قوة الرابطة بين الأكسجين والهيموجلوبين (بالإضافة إلى أنها تمثل "قيمة مرجعية مهمة في تنظيم التهوية الرئوية).
بتلخيص كل شيء بالرسم البياني ، فإن كمية الأكسجين المرتبطة بالهيموجلوبين تنمو فيما يتعلق بـ pO2 بعد منحنى السيني:

حقيقة أن منطقة اللوح كبيرة جدًا تضع هامش أمان مهمًا عند أقصى تشبع للهيموجلوبين أثناء المرور إلى الرئتين. على الرغم من أن pO2 في المستوى السنخي عادةً ما يساوي 100 مم زئبق ، مع ملاحظة الشكل نلاحظ في الواقع كيف حتى الضغط الجزئي للأكسجين يساوي 70 مم زئبق (حدوث نموذجي لبعض الأمراض أو البقاء على ارتفاعات عالية) ، تظل نسب الهيموجلوبين المشبع قريبة من 100٪.
في منطقة الانحدار الأقصى ، عندما ينخفض التوتر الجزئي للأكسجين عن 40 مم زئبق ، تنخفض قدرة الهيموجلوبين على الارتباط بالأكسجين فجأة.
في ظروف الراحة ، يكون PO2 في السوائل داخل الخلايا حوالي 40 مم زئبق ؛ في هذا الموقع ، بسبب قوانين الغازات ، ينتشر الأكسجين المذاب في البلازما نحو الأنسجة الأكثر فقراً من O2 ، عابراً غشاء الشعيرات الدموية ، وبالتالي ينخفض توتر البلازما لـ O2 بشكل أكبر ، وهذا يفضل إطلاق الأكسجين من الهيموجلوبين. . أثناء المجهود البدني المكثف ، من ناحية أخرى ، ينخفض توتر الأكسجين في الأنسجة إلى 15 مم زئبق أو أقل ، ونتيجة لذلك ينضب الدم من الأكسجين بشكل كبير.
لما قيل ، في ظروف الراحة تترك كمية كبيرة من الهيموجلوبين المؤكسج الأنسجة ، وتبقى متوفرة عند الحاجة (على سبيل المثال للتعامل مع الزيادة المفاجئة في التمثيل الغذائي في بعض الخلايا).
يسمى الخط الصلب الموضح في الصورة أعلاه بمنحنى تفكك الهيموجلوبين. يتم تحديده عادة في المختبر عند درجة الحموضة 7.4 وعند درجة حرارة 37 درجة مئوية.
تأثير بوهر له عواقب على تناول O2 على مستوى الرئة وعلى إطلاقه على مستوى الأنسجة.
عندما يكون هناك المزيد من ثاني أكسيد الكربون المذاب على شكل بيكربونات ، فإن الهيموجلوبين يطلق الأكسجين بسهولة أكبر ويصبح مشحونًا بثاني أكسيد الكربون (على شكل بيكربونات).

يتم الحصول على نفس التأثير عن طريق تحمض الدم: كلما انخفض الرقم الهيدروجيني في الدم وظل الأكسجين مرتبطًا بالهيموجلوبين ؛ وليس من المستغرب أن يتحلل ثاني أكسيد الكربون في الدم بشكل أساسي على شكل حمض الكربونيك ، الذي ينفصل.



تكريما لمكتشفه ، يُعرف تأثير الأس الهيدروجيني أو ثاني أكسيد الكربون على تفكك الأكسجين باسم تأثير بوهر.
كما هو متوقع ، في البيئة الحمضية ، يطلق الهيموجلوبين الأكسجين بسهولة أكبر ، بينما في البيئة الأساسية تكون الرابطة مع الأكسجين أقوى.

العوامل الأخرى القادرة على تعديل انجذاب الهيموجلوبين للأكسجين تشمل درجة الحرارة. على وجه الخصوص ، تقل ألفة الهيموجلوبين للأكسجين مع زيادة درجة حرارة الجسم. وهذا مفيد بشكل خاص خلال أشهر الشتاء والربيع ، حيث أن درجة حرارة الدم الرئوي (عند التلامس مع هواء البيئة الخارجية) أقل مما يتم الوصول إليه في الأنسجة ، حيث يسهل بالتالي إطلاق الأكسجين.

2.3 diphosphoglycerate هو وسيط في تحلل السكر الذي يؤثر على تقارب الهيموجلوبين للأكسجين. إذا زادت تركيزاته داخل خلايا الدم الحمراء ، فإن تقارب الهيموجلوبين للأكسجين ينخفض ، مما يسهل إطلاق الأكسجين إلى الأنسجة. وليس من المستغرب أن تكون تركيزات كرات الدم الحمراء من 2،3 ثنائي فسفوغليسيرات زيادة ، على سبيل المثال ، في فقر الدم ، وقصور القلب والرئتين وأثناء الإقامة على ارتفاعات عالية.
بشكل عام ، يكون تأثير 2،3 بيسفوسفوجليسيرات بطيئًا نسبيًا ، خاصة عند مقارنته بالاستجابة السريعة للتغيرات في درجة الحموضة ودرجة الحرارة والضغط الجزئي لثاني أكسيد الكربون.

تأثير بوهر مهم للغاية أثناء العمل العضلي المكثف ؛ في مثل هذه الظروف ، في الواقع ، في الأنسجة الأكثر تعرضًا للإجهاد ، هناك زيادة محلية في درجة حرارة وضغط ثاني أكسيد الكربون ، وبالتالي في حموضة الدم. كما هو موضح أعلاه ، كل هذا يفضل إطلاق الأكسجين إلى الأنسجة ، مما يؤدي إلى تحويل منحنى تفكك الهيموجلوبين إلى اليمين.