لكي تكون قادرًا على التحدث بطريقة مفهومة "الهيموغلوبين (خضاب الدم)، من المفيد أن تهتم بالأول ميوغلوبين (ميغابايت) وهو مشابه جدًا للهيموجلوبين ولكنه أبسط بكثير.بين الهيموجلوبين والميوجلوبين توجد علاقات قرابة وثيقة: كلاهما بروتينات مترافقة ومجموعة الأطراف الاصطناعية (جزء غير بروتيني) هي المجموعة الهيم.
الميوجلوبين هو بروتين كروي يتكون من سلسلة واحدة من حوالي مائة وخمسين حمضًا أمينيًا (يعتمد على الكائن الحي) ويبلغ وزنه الجزيئي حوالي 18 كيلو دالتون.
كما ذكرنا ، فهي مجهزة بمجموعة هيم يتم إدخالها في جزء مسعور (أو محب للدهون) من البروتين ، وتتكون من طيات تُعزى إلى الهياكل الحلزونية α للبروتينات الليفية.
يتكون الميوغلوبين بشكل أساسي من أجزاء من حلزونات ألفا ، موجودة في عدد ثمانية وتتكون ، بشكل حصري تقريبًا ، من بقايا غير قطبية (ليوسين ، فالين ، ميثيونين وفينيل ألانين) بينما البقايا القطبية غائبة عمليًا (حمض الأسبارتيك ، حمض الجلوتاميك ، ليسين و أرجينين) ؛ البقايا القطبية الوحيدة هي نوعان من الهيستدين ، اللذان يلعبان دورًا أساسيًا في ربط الأكسجين بمجموعة الهيم.
مجموعة الهيم هي مجموعة كروموفور (تمتص في المرئي) وهي المجموعة الوظيفية للميوجلوبين.
أنظر أيضا: الهيموجلوبين السكري - الهيموجلوبين في البول
القليل من الكيمياء

الرابطة بين البروتوبورفيرين والحديد هي رابطة نموذجية لمركبات التنسيق وهي مركبات كيميائية تشكل فيها ذرة مركزية (أو أيون) روابط مع أنواع كيميائية أخرى بعدد أكبر من رقم تأكسدها (شحنة كهربائية). في حالة الهيم ، تكون هذه الروابط ضعيفة وقابلة للانعكاس.
رقم التنسيق (عدد روابط التنسيق) للحديد هو ستة: يمكن أن يكون هناك ستة جزيئات حول الحديد تشترك في إلكترونات الرابطة.
لتشكيل مركب تنسيق ، يتطلب الأمر مدارين مع اتجاه صحيح: أحدهما قادر على "اكتساب" الإلكترونات والآخر قادر على التبرع بها.
في الهيم ، يشكل الحديد أربع روابط مستوية مع أربع ذرات نيتروجين في مركز حلقة بروتو بورفيرين ورابطة خامسة مع نيتروجين هيستيدين قريب ؛ يحتوي الحديد على سادس رابطة تنسيق حرة ويمكنه الارتباط بالأكسجين.
عندما يكون الحديد في شكل أيون حر ، يكون نوعه مدارات د لديهم جميعًا نفس الطاقة ؛ في الميوجلوبين ، يرتبط أيون الحديد بالبروتوبورفيرين والهيستيدين: هذه الأنواع تزعج المدارات مغناطيسيًا د بعض الحديد سيكون مدى الاضطراب مختلفًا بالنسبة للمدارات المختلفة د اعتمادًا على اتجاهها المكاني واتجاه الأنواع المقلقة. نظرًا لأن الطاقة الإجمالية للمدارات يجب أن تكون ثابتة ، فإن الاضطراب يؤدي إلى فصل نشط بين المدارات المختلفة: الطاقة المكتسبة من قبل بعض المدارات تعادل الطاقة المفقودة من قبل الآخرين.
إذا لم يكن الفصل الذي يحدث بين المدارات كبيرًا جدًا ، فمن الأفضل ترتيبًا إلكترونيًا عالي الدوران: تحاول الإلكترونات الملزمة ترتيب نفسها في لفات متوازية في أكبر عدد ممكن من المستويات الفرعية (أقصى تعدد) ؛ من ناحية أخرى ، إذا كان الاضطراب قويًا جدًا وكان هناك فاصل كبير بين المدارات ، فقد يكون من الأنسب إقران إلكترونات الرابطة في مدارات الطاقة المنخفضة (الدوران المنخفض).
عندما يرتبط الحديد بالأكسجين ، يفترض الجزيء ترتيب دوران منخفض بينما عندما يكون للحديد رابطة التنسيق السادسة خالية ، يكون للجزيء ترتيب دوران عالي.
بفضل هذا الاختلاف في الدوران ، من خلال التحليل الطيفي للميوغلوبين ، يمكننا أن نفهم ما إذا كان الأكسجين (MbO2) مرتبطًا به أم لا (ميغابايت).
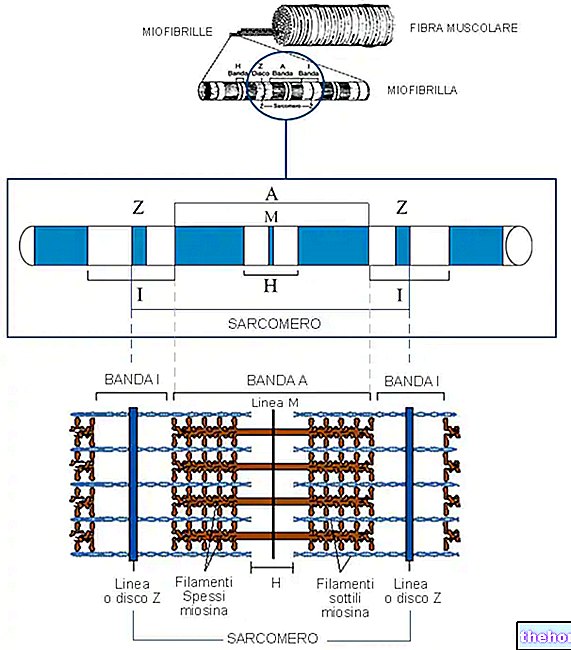
الميوغلوبين هو بروتين عضلي نموذجي (لكنه لا يوجد فقط في العضلات).
يُستخرج الميوغلوبين من حوت العنبر الذي يوجد فيه بكميات كبيرة ثم يتم تنقيته.
تتنفس الحوتيات مثل تلك التي يتنفسها البشر: فلديها رئتان يجب أن تمتص الهواء من خلال عملية التنفس ؛ يجب أن يجلب حوت العنبر أكبر قدر ممكن من الأكسجين إلى العضلات القادرة على تجميع الأكسجين عن طريق ربطه بالميوجلوبين الموجود فيها ؛ ثم يتم إطلاق الأكسجين ببطء عند غمر الحيتانيات لأن عملية الأيض تتطلب الأكسجين: كلما زادت الكمية من الأكسجين الذي يستطيع حوت العنبر امتصاصه ويتوفر المزيد من الأكسجين أثناء الغوص.
يربط Myoglybin الأكسجين بطريقة قابلة للعكس ويوجد في الأنسجة المحيطية بنسبة أكبر كلما زاد استخدام الأنسجة للعمل مع إمدادات الأكسجين البعيدة في الوقت المناسب.
<--- الميوغلوبين هو بروتين موجود في العضلات ، وظيفته هي بالضبط وظيفة "خزان" الأكسجين.
ما يجعل اللحم أحمر أكثر أو أقل هو محتوى البروتينات الدموية (الهيم هو الذي يجعل اللحم أحمر).
يحتوي الهيموغلوبين على العديد من أوجه التشابه البنيوية مع الميوغلوبين وهو قادر على ربط الأكسجين الجزيئي بطريقة قابلة للعكس ؛ ولكن ، بينما يقتصر الميوغلوبين على العضلات والأنسجة الطرفية بشكل عام ، يوجد الهيموجلوبين في كريات الدم الحمراء أو خلايا الدم الحمراء (وهي خلايا زائفة ، أي أنها ليست خلايا حقيقية) التي تشكل 40٪ من الدم.
على عكس الميوجلوبين ، فإن عمل الهيموجلوبين هو أخذ الأكسجين في الرئتين ، وإطلاقه في الخلايا حيث تكون هناك حاجة إليه ، وأخذ ثاني أكسيد الكربون وإطلاقه في الرئتين حيث تبدأ الدورة مرة أخرى.
L "الهيموغلوبين إنه مقياس رباعي ، أي أنه يتكون من أربعة سلاسل بولي ببتيد كل منها مع مجموعة هيم ومتطابقة اثنين في اثنين (في الإنسان هناك سلسلتان ألفا وسلسلتان بيتا).
تتمثل الوظيفة الرئيسية للهيموجلوبين في نقل الأكسجين ؛ وظيفة أخرى للدم الذي يشارك فيه الهيموجلوبين هي نقل المواد إلى الأنسجة.
في المسار من الرئتين (الغني بالأكسجين) إلى الأنسجة ، يحمل الهيموجلوبين الأكسجين (في نفس الوقت تصل المواد الأخرى إلى الأنسجة) بينما في المسار العكسي يحمل معه النفايات التي تجمعها الأنسجة ، وخاصة الكربون ينتج ثاني أكسيد في عملية التمثيل الغذائي.
في تطور الإنسان توجد جينات يتم التعبير عنها فقط لفترة زمنية معينة ؛ لهذا السبب توجد الهيموجلوبين المختلف: الجنين ، الجنين ، للرجل البالغ.
السلاسل التي تتكون منها هذه الهيموجلوبينات المختلفة لها هياكل مختلفة ولكن مع بعض أوجه التشابه في الواقع فإن الوظيفة التي تؤديها هي نفسها إلى حد ما.
شرح لوجود العديد من السلاسل المختلفة هو ما يلي: في سياق العملية التطورية للكائنات الحية ، حتى الهيموجلوبين قد تطور متخصصًا في نقل الأكسجين من المناطق الغنية به إلى المناطق التي تعاني من نقص. في "البداية" من السلسلة التطورية l "الهيموجلوبين ينقل الأكسجين في الكائنات الحية الصغيرة ؛ في سياق التطور وصلت الكائنات الحية إلى أبعاد أكبر ، لذلك تم تعديل الهيموجلوبين ليكون قادرًا على نقل الأكسجين إلى مناطق أبعد من النقطة التي كان فيها غنيًا به ؛ إلى عند القيام بذلك تم ترميزهم ، في سياق العملية التطورية ، هياكل جديدة من السلاسل التي تتكون منها الهيموجلوبين.
يربط الميوغلوبين الأكسجين حتى عند الضغوط المتواضعة ؛ في الأنسجة المحيطية يوجد ضغط (PO2) يبلغ حوالي 30 ملم زئبقي: الميوغلوبين عند هذا الضغط لا يطلق الأكسجين ، لذلك سيكون غير فعال كحامل للأكسجين. الهيموغلوبين ، من ناحية أخرى ، لديه سلوك أكثر مرونة: فهو يربط الأكسجين بالضغوط العالية ويطلقه عندما ينخفض الضغط.
عندما يكون البروتين نشطًا وظيفيًا ، يمكنه تغيير شكله قليلاً ؛ على سبيل المثال ، يكون للميوغلوبين المؤكسج شكل مختلف عن الميوغلوبين غير المؤكسج ولا تؤثر هذه الطفرة على جيرانه.
يختلف الوضع في حالة البروتينات المصاحبة مثل الهيموجلوبين: عندما تتأكسج سلسلة ، يتم تحفيزها لتغيير شكلها ولكن هذا التعديل ثلاثي الأبعاد لذلك تتأثر أيضًا السلاسل الأخرى للمقياس الرباعي. حقيقة أن السلاسل مرتبطة مع بعضها البعض. ، يشير إلى أن تعديل أحدهما يؤثر على الجيران الآخرين حتى لو كان إلى حد مختلف ؛ عندما تتأكسج سلسلة ، تفترض السلاسل الأخرى للمقياس الرباعي "موقفًا أقل عدائية" تجاه الأكسجين: الصعوبة التي تواجهها السلسلة يتناقص الأكسجين حيث تتأكسج السلاسل القريبة منه. الشيء نفسه ينطبق على نزع الأكسجين.
يُطلق على التركيب الرباعي لـ deoxyhemoglobin شكل T (متوتر) بينما يسمى هيكل أوكسي هيموغلوبين R (تم إطلاقه) ؛ في حالة التوتر ، توجد سلسلة من التفاعلات الكهروستاتيكية القوية بين الأحماض الأمينية الحمضية والأحماض الأمينية الأساسية التي تؤدي إلى بنية صلبة من deoxyhemoglobin (وهذا هو السبب في "الشكل المتوتر") ، بينما عندما يرتبط الأكسجين ، فإن كيان هذه التفاعلات تتناقص (ومن هنا جاء "النموذج المفرج"). علاوة على ذلك ، في حالة عدم وجود الأكسجين ، يتم تثبيت شحنة الهيستيدين (انظر التركيب) بواسطة الشحنة المعاكسة لحمض الأسبارتيك ، بينما في وجود الأكسجين ، هناك ميل من جانب البروتين إلى فقد البروتون ؛ كل هذا ينطوي على أن الهيموغلوبين المؤكسج هو حمض أقوى من الهيموغلوبين غير المؤكسج: تأثير بوهر.
اعتمادًا على الرقم الهيدروجيني ، ترتبط مجموعة الهيم بالأكسجين بسهولة أكبر أو أقل: في البيئة الحمضية ، يطلق الهيموغلوبين الأكسجين بسهولة أكبر (يكون الشكل المتوتر مستقرًا) بينما ، في البيئة الأساسية ، يكون الارتباط بالأكسجين أكثر صعوبة.

يطلق كل هيموجلوبين 0.7 بروتون لكل مول من الأكسجين (O2) يدخل.
يسمح تأثير بوهر للهيموجلوبين بتحسين قدرته على حمل الأكسجين.
يجب أن يوازن الهيموغلوبين الذي ينتقل من الرئتين إلى الأنسجة نفسه كدالة للضغط ودرجة الحموضة ودرجة الحرارة.
دعونا نرى تأثير درجة الحرارة.
درجة الحرارة في الحويصلات الهوائية الرئوية أقل بحوالي 1-1.5 درجة مئوية من درجة الحرارة الخارجية بينما تكون درجة الحرارة في العضلات حوالي 36.5-37 درجة مئوية ؛ مع ارتفاع درجة الحرارة ، ينخفض عامل التشبع (عند نفس الضغط): يحدث هذا بسبب زيادة الطاقة الحركية ويفضل التفكك.

هناك عوامل أخرى يمكن أن تؤثر على قدرة الهيموجلوبين على الارتباط بالأكسجين ، أحدها تركيز 2،3 بيسفوسفوجليسيرات.
2،3 بيسفوسفوجليسيرات هو التمثيل الغذائي الموجود في كريات الدم الحمراء بتركيز 4-5 ملي مولار (لا يوجد في أي جزء آخر من الكائن الحي في مثل هذا التركيز العالي).
في درجة الحموضة الفسيولوجية ، يتم نزع 2،3 من البايفوسفوجليسيرات ولديها خمس شحنات سلبية ؛ وهو محصور بين سلسلتي بيتا من الهيموجلوبين لأن هذه السلاسل تحتوي على تركيز عالٍ من الشحنات الموجبة. تمنح التفاعلات الكهروستاتيكية بين سلاسل بيتا و 2،3 بيسفوسفوجليسرات صلابة معينة للنظام: يتم الحصول على بنية متوترة ذات تقارب ضئيل للأكسجين ؛ أثناء الأوكسجين ، يتم طرد 2،3 بيسفوسفوجليسيرات.
في كريات الدم الحمراء c "عبارة عن جهاز خاص يحول 1.3 bisphosphoglycerate (ينتج عن طريق التمثيل الغذائي) إلى 2.3 bisphosphoglycerate بحيث يصل تركيزه إلى 4-5 ملي مولار وبالتالي فإن الهيموجلوبين قادر على تبادل" الأكسجين في الأنسجة.
يكون الهيموغلوبين الذي يصل إلى الأنسجة في حالة إطلاق (مرتبط بالأكسجين) ، ولكن بالقرب من النسيج ، يكون كربوكسيل ويمر إلى الحالة المتوترة: البروتين في هذه الحالة يكون أقل ميلًا للارتباط بالأكسجين ، فيما يتعلق إلى الحالة المنبعثة ، وبالتالي يطلق الهيموغلوبين الأكسجين إلى الأنسجة ؛ علاوة على ذلك ، من خلال التفاعل بين الماء وثاني أكسيد الكربون ، هناك إنتاج أيونات H + ، وبالتالي المزيد من الأكسجين بسبب تأثير بوهر.
ينتشر ثاني أكسيد الكربون في كرات الدم الحمراء التي تمر عبر غشاء البلازما. بما أن كريات الدم الحمراء تشكل حوالي 40٪ من الدم ، يجب أن نتوقع أن 40٪ فقط من ثاني أكسيد الكربون الذي ينتشر من الأنسجة يدخلها ، في الواقع 90٪ من ثاني أكسيد الكربون يدخل كريات الدم الحمراء لأنها تحتوي على إنزيم يحول ثاني أكسيد الكربون. في حمض الكربونيك ، ينتج عن ذلك أن التركيز الثابت لثاني أكسيد الكربون في كريات الدم الحمراء منخفض وبالتالي يكون معدل الدخول مرتفعًا.

ظاهرة أخرى تحدث عندما تصل كريات الدم الحمراء إلى نسيج هي ما يلي: بالتدرج ، يترك "HCO3- (مشتق من ثاني أكسيد الكربون)" كريات الدم الحمراء ، ولموازنة ناتج الشحنة السالبة ، لدينا "دخول الكلوريدات التي يحدد زيادة في الضغط التناضحي: لموازنة هذا الاختلاف ، يوجد أيضًا دخول الماء الذي يسبب تورم كريات الدم الحمراء (تأثير هامبرجر). تحدث الظاهرة المعاكسة عندما تصل كريات الدم الحمراء إلى الحويصلات الرئوية: انكماش كريات الدم الحمراء (تأثير هالدان) لذلك فإن كريات الدم الحمراء الوريدية (الموجهة إلى الرئتين) تكون أكثر استدارة من الخلايا الشريانية.


.jpg)





















.jpg)

